题目内容
1.(1)写出以下物质的结构简式或命名2,3-二甲基-4-乙基已烷:
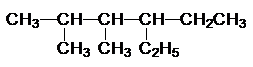 ; TNT:
; TNT: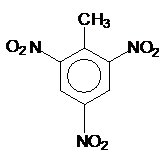 ;
;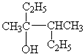 :3,4-二甲基-3-己醇,
:3,4-二甲基-3-己醇,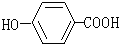 :对羟基苯甲酸.
:对羟基苯甲酸.(2)某有机分子结构如下:
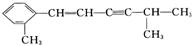 该分子中最多有13个C原子共处同一平面
该分子中最多有13个C原子共处同一平面(3)工程塑料ABS树脂合成时用了三种单体.ABS树脂的结构简式如图所示,这三种单体的结构简式分别是CH2=CHCN、CH2=CH-CH=CH、
 .
.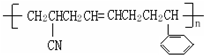
(4)将C8H18完全裂化,生成的产物中只有C4H8、CH4、C3H6、C2H6、C2H4,则气体产物的平均相对分子量为28.5<M≤38.
(5)400K、101.3kPa时,1.5L某烃蒸气能在aL氧气中完全燃烧,体积增大至(a+3)L(相同条件下).该烃在组成上必须满足的基本条件是CxH8.
分析 (1)2,3-二甲基-4-乙基已烷,主链有6个碳原子的烷烃,2、3号碳原子上各有1个甲基,4号碳原子上有1个乙基;
TNT是烈性炸药系统命名为2,4,6-三硝基甲苯;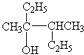 为主链有6个碳原子的醇,从左端编号,醇羟基在3号碳原子上,3、4号碳原子上各有1个甲基;
为主链有6个碳原子的醇,从左端编号,醇羟基在3号碳原子上,3、4号碳原子上各有1个甲基;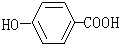 苯环的对位上连接一个羟基,一个羧基;
苯环的对位上连接一个羟基,一个羧基;
(2)依据苯为平面正六边形结构、乙烯为平面型结构、乙炔为线型结构,当苯环与乙烯处于同一平面时共面的碳原子最多;
(3)首先要根据高聚物的结构简式判断高聚物是加聚产物还是缩聚产物,然后根据推断单体的方法作出判断;
(4)根据C原子、H原子守恒,判断C8H18裂化可能发生的反应情况,根据反应情况判断1molC8H18裂化所得的混合气体的物质的量的范围,再根据极限法计算平均相对分子质量的范围;
(5)依据烃燃烧的通式400K时,生成的水为气态,根据烃燃烧通式CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O,利用气体体积差量计算.
解答 解:(1)2,3-二甲基-4-乙基已烷,主链有6个碳原子的烷烃,2、3号碳原子上各有1个甲基,4号碳原子上有1个乙基,其结构简式为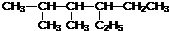 ;
;
TNT是烈性炸药系统命名为2,4,6-三硝基甲苯,结构简式为: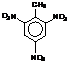 ;
; 为主链有6个碳原子的醇,从左端编号,醇羟基在3号碳原子上,3、4号碳原子上各有1个甲基,系统命名为:3,4-二甲基-3-己醇;
为主链有6个碳原子的醇,从左端编号,醇羟基在3号碳原子上,3、4号碳原子上各有1个甲基,系统命名为:3,4-二甲基-3-己醇; 苯环的对位上连接一个羟基,一个羧基,习惯命名为:对羟基苯甲酸;
苯环的对位上连接一个羟基,一个羧基,习惯命名为:对羟基苯甲酸;
故答案为: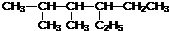
 ;3,4-二甲基-3-己醇;对羟基苯甲酸;
;3,4-二甲基-3-己醇;对羟基苯甲酸;
(2)当苯环与乙烯处于同一平面时共面的碳原子最多,最多有13个,分别为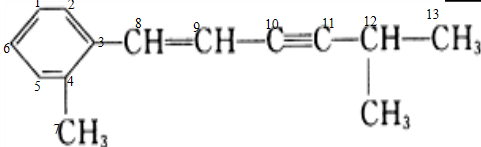 ;
;
故答案为:13;
(3)该高聚物的形成过程属于加聚反应,加聚反应是由不饱和单体(如碳碳双键,碳碳叁键以及碳氧双键等)聚合高分子的反应,其产物只有一种高分子化合物,凡链节中主碳链为6个碳原子,其规律是“见双键,四个碳,无双键,两个碳”画线断开,然后将半键闭合,即将单双键互换,直接合成该高聚物的物质为:CH2=CH-CN、CH2=CH-CH=CH2、 ,故答案为:CH2=CHCN;CH2=CH-CH=CH2;
,故答案为:CH2=CHCN;CH2=CH-CH=CH2;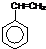 ;
;
(4)按照题目所给C8H18的裂化产物考虑,C8H18裂化可能发生的反应共有以下几种:
①C8H18→C4H8+C3H6+CH4
②C8H18→C4H8+C2H4+C2H6
③C8H18→2C3H6+C2H6
④C8H18→C3H6+2C2H4+CH4
⑤C8H18→3C2H4+C2H6
以上反应①、②、③是1molC8H18裂化生成3mol混合气体;④、⑤反应是1molC8H18裂化生成4mol混合气体.要得到题目所述的混合气体,按①、②、③反应就可以实现;但是按④、⑤反应并不能得到题目所述的混合气体,至少需要①、②中的一个反应参与或者共同参与,③也有可能同时参与.
这样1molC8H18裂化所得的混合气体的物质的量为3mol≤n<4mol,所以混合气体的平均摩尔质量$\frac{1mol×114g/mol}{4mol}$<Mr≤$\frac{1mol×114g/mol}{3mol}$,
即平均相对分子质量为28.5<Mr≤38,故答案为:28.5<Mr≤38;
(5)设烃的分子式为CxHy,则:
CxHy+(x+$\frac{y}{4}$)O2$\stackrel{点燃}{→}$xCO2+$\frac{y}{2}$H2O 气体体积差量△V
1 (x+$\frac{y}{2}$-x-$\frac{y}{4}$-1)
1.5 (a+3-a-1.5)
解得:y=8;
即该烃的分子式为:CxH8;故答案为:CxH8.
点评 本题考查较综合,涉及有机物的命名、结构与性质、烃燃烧的规律,侧重考查学生的综合能力和计算能力,题目难度中等.

| A. | 室温下,22.0g C18O2气体中含有的碳原子数目为0.5NA | |
| B. | 1mol OH-中电子数为10NA | |
| C. | 标准状况下,22.4L乙醇中含有的氧原子数为1.0NA | |
| D. | 1mol C2Cl6分子含有7 NA个共价键 |
| A. | 反应体系的总压恒定 | B. | A、B、C、D的物质的量之比为1:3:2:2 | ||
| C. | c(A):c(B)=1:3 | D. | 2V(B)正=3V(C)逆 |
| A. | 烃的组成均符合通式CnH2n+2 | |
| B. | 烃类均不溶于水 | |
| C. | 甲烷在烃中含碳量最低 | |
| D. | 甲烷只能发生取代反应而不能发生加成反应 |
| X | Y | |
| Z | W |
(1)W位于周期表中第三周期,第ⅦA族.
(2)X和氢可以构成+1价阳离子,其电子式是
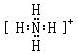 ,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).
,Y的气态氢化物的稳定性比Z的气态氢化物的稳定性强(填“强”、或“弱”).(3)X的最高价氧化物的水化物与其氢化物能化合生成M,M的水溶液显酸性的原因是NH4++H2O?NH3•H2O+H+(用离子方程式表示).
(4)①Y和Z可组成一种气态化合物Q,Q能与W的单质在潮湿环境中反应,反应的化学方程式是SO2+Cl2+2H2O=2HCl+H2SO4.
②在一定条件下,化合物Q与Y的单质反应达平衡时有三种气态物质,反应时,每转移4mol电子放热190.0kJ,该反应的热化学方程式是2SO2 (g)+O2(g)?2SO3(g)△H=-190.0 kJ•mol-1.
| A. | K+ Na+ OH- SO42- | B. | Mg2+ SO42- NH4+ Cl- | ||
| C. | K+ Na+ HCO3- Cl- | D. | K+ Na+ NO3- CO32- |
(1)H+的物质的量 (2)c(H+) (3)c(OH-) (4)$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$ (5)$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$.
| A. | (1)(3)(4) | B. | (1)(3)(5) | C. | (2)(4)(5) | D. | (1)(4)(5) |
| A. | 其单质在常温下为白色固体 | |
| B. | 原子的最外电子层上有7个电子 | |
| C. | 其最高价氧化物对应水化物一定为强酸 | |
| D. | 其元素位于元素周期表中第五周期第 VII族 |