题目内容
17.下列说法正确的是( )| A. | 硅元素主要以单质、氧化物、硅酸盐的形式存在于自然界 | |
| B. | 浓氨水中滴加FeCl3饱和溶液可制得Fe(OH)3胶体 | |
| C. | 医药中,常用酒精来消毒,是因为酒精能够使细菌蛋白质发生变性 | |
| D. | Ca(HCO3)2溶液与过量NaOH溶液反应可制得Ca(OH)2 |
分析 A.自然界中不存在游离态硅;
B.浓氨水中滴加FeCl3饱和溶液,反应生成氢氧化铁沉淀;
C.有机物能够使蛋白质变性;
D.Ca(HCO3)2溶液与过量NaOH溶液反应生成碳酸钙、碳酸钠和水.
解答 解:A.硅在自然界中以化合态存在,不存在游离态硅,故A错误;
B.浓氨水中滴加FeCl3饱和溶液反应生成氢氧化铁沉淀,得不到Fe(OH)3胶体,故B错误;
C.细菌属于蛋白质,酒精能够使蛋白质变性,所以酒精能够杀菌消毒,故C正确;
D.Ca(HCO3)2溶液与过量NaOH溶液反应生成碳酸钙、碳酸钠和水,得不到氢氧化钙,故D错误;
故选:C.
点评 本题考查了元素化合物知识,熟悉硅、胶体、蛋白质的性质即可解答,题目难度不大.

练习册系列答案
相关题目
5.下列物质的性质比较,正确的是( )
| A. | 酸性:H2SO4>HClO4 | B. | 碱性:NaOH>KOH | ||
| C. | 非金属性:P>S | D. | 气态氢化物稳定性:HCl>H2S |
12.下列实验装置图,其中关于用途的描述,不正确的是( )
| A. |  装置:收集二氧化碳,从a口进气b口排气 | |
| B. | 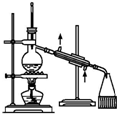 装置:用于石油的分馏 | |
| C. | 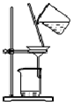 装置:用于分离Cl2与KI溶液反应生成的碘 | |
| D. | 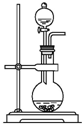 装置:可用来制取氨气 |
2.下列有关化学实验操作的说法不合理的是( )
| A. | 在配制FeSO4溶液时常向其中加入一定量铁粉和稀硫酸 | |
| B. | 用广泛pH试纸测量得某溶液的pH=13 | |
| C. | 用碱式滴定管量取20.00mL0.1000mol/LKmnO4溶液 | |
| D. | 实验室可将铜先氧化成氧化铜,再与硫酸反应来制取硫酸铜以节约药品、减少污染 |
9.伞形酮可用作荧光指示剂和酸碱指示剂,其合成方法如图所示,下列有关这三种物质的说法正确的是( )


| A. | 雷琐苯乙酮所有碳原子不可能共平面 | |
| B. | 雷琐苯乙酮、伞形酮能用酸性KmnO4鉴别 | |
| C. | 1mol雷琐苯乙酮跟足量H2反应,最多消耗3molH2 | |
| D. | 1mol伞形酮与足量NaOH溶液反应,最多消耗3molNaOH |
6.下列叙述中,不正确的是( )
| A. | Al(OH)3胶体能疑凝聚水中悬浮物 | |
| B. | 铝易被氧化,但氧化生成的氧化铝具有保护内部铝的作用 | |
| C. | 铝是地壳中含量最多的金属元素 | |
| D. | Al(OH)3能溶于NaOH溶液、氨水和稀硫酸 |
7.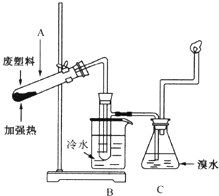 某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:
某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:
(1)试管A中残余物有多种用途,如下列转化就可制取高聚物聚乙炔.

写出反应②、③的化学方程式CaC2+2H2O→Ca(OH)2+C2H2↑,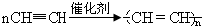 .
.
(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有4种.
(3)锥形瓶C中观察到的现象是棕黄色溶液变无色或褪色,经溴水充分吸收后,剩余气体经干燥后平均相对分子质量为4.8.
(4)写出C中逸出的气体在工业上的两种用途合成氨原料、作燃料或有机化工原料.
 某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:
某些废旧塑料可采用下列方法处理,将废塑料隔绝空气加强热,使其变成有用的物质,实验装置如图所示.加热聚丙烯废塑料得到的产物如下表所示:| 产物 | 氢气 | 甲烷 | 乙烯 | 丙烯 | 苯 | 甲苯 | 炭 |
| 质量分数(%) | 12 | 24 | 12 | 16 | 20 | 10 | 6 |

写出反应②、③的化学方程式CaC2+2H2O→Ca(OH)2+C2H2↑,
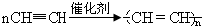 .
.(2)试管B收集到的产品中,能使酸性高锰酸钾溶液褪色的物质,其一氯代物有4种.
(3)锥形瓶C中观察到的现象是棕黄色溶液变无色或褪色,经溴水充分吸收后,剩余气体经干燥后平均相对分子质量为4.8.
(4)写出C中逸出的气体在工业上的两种用途合成氨原料、作燃料或有机化工原料.
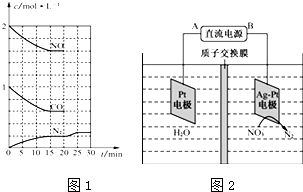
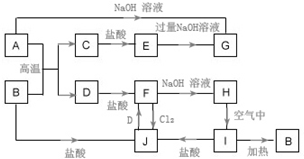 A~J为中学化学的常见物质,它们之间有如图所示的转化关系(部分产物已略去).已知A、D为金属单质,B为红棕色粉末,I为红褐色固体.
A~J为中学化学的常见物质,它们之间有如图所示的转化关系(部分产物已略去).已知A、D为金属单质,B为红棕色粉末,I为红褐色固体.