题目内容
15.实验室有瓶混有泥沙的乙二酸样品,小明利用这个反应的原理来测定其含量,操作为:①配制250mL溶液:准确称量5.0g乙二酸样品,配成250mL溶液.
②滴定:准确量取25.00mL所配溶液于锥形瓶中,加少量酸酸化,将0.1000mol•L-1KMnO4溶液装入酸式(填“酸式”或“碱式”)滴定管,进行滴定操作.在实验中发现,刚滴下少量KMnO4溶液时,溶液迅速变成紫红色.将锥形瓶摇动一时间后,紫红色慢慢消失;再继续滴加时,紫红色就很快褪色了.请解释原因:反应中生成的锰离子具有催化作用,所以随后褪色会加快.当滴入最后一滴高锰酸钾溶液,锥形瓶内的颜色由无色变成紫红色,且半分钟不变化,证明达到滴定终点.
③计算:再重复上述操作2次,记录实验数据如下.
| 序号 | 滴定前读数(mL) | 滴定后读数(mL) |
| 1 | 0.00 | 20.10 |
| 2 | 1.00 | 20.90 |
| 3 | 0.00 | 22.10 |
④误差分析:下列操作会导致测定结果偏高的是ACD.
A.未用标准浓度的酸性KMnO4溶液润洗滴定管
B.滴定前锥形瓶有少量水
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失
D.不小心将少量酸性KMnO4溶液滴在锥形瓶外
E.观察读数时,滴定前仰视,滴定后俯视.
分析 ②KMnO4溶液具有强氧化性,应用酸式滴定管盛装;高锰离子有催化作用而导致反应速率加快;乙二酸与KMnO4发生氧化还原反应,滴定终点时,溶液由无色变成紫红色,且半分钟内不褪色;
③第3组KMnO4溶液的体积与第1、2组相差比较大,舍去第3组,应按第1、2组的平均值为消耗KMnO4溶液的体积,根据关系式2KMnO4~5H2C2O4计算;
④根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析不当操作对V(标准)的影响,以此判断浓度的误差.
解答 解:②KMnO4溶液具有强氧化性,应用酸式滴定管盛装;高锰酸根离子被还原生成的锰离子有催化作用而导致反应速率加快,所以刚滴下少量KMnO4溶液时,溶液迅速变成紫红色;滴定终点时,当滴入最后一滴高锰酸钾溶液,锥形瓶内的颜色由无色变成紫红色,且半分钟不变化,证明达到终点;
故答案为:酸式;反应中生成的锰离子具有催化作用,所以随后褪色会加快;滴入最后一滴高锰酸钾溶液,锥形瓶内的颜色由无色变成紫红色,且半分钟不变化;
③第3组KMnO4溶液的体积与第1、2组相差比较大,舍去第3组,应按第1、2组的平均值为消耗KMnO4溶液的体积,故消耗KMnO4溶液的体积为$\frac{20.10+19.90}{2}$mL=20mL
设样品的纯度为x,
5H2C2O4 +2MnO4-+6H+=10CO2↑+2Mn2++8H2O
450g 2mol
5.0g×x×$\frac{1}{10}$g (0.1000×0.020)mol
解得:x=$\frac{0.1×0.020×450}{2×5.0×0.1}$=90.00%,
故答案为:20.00;90.00%;
④A.未用标准浓度的酸性KMnO4溶液润洗滴定管,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,c(标准)偏大,故A正确;
B.滴定前锥形瓶有少量水,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,c(标准)不变,故B错误;
C.滴定前滴定管尖嘴部分有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,c(标准)偏大,故C正确;
D.不小心将少量酸性KMnO4溶液滴在锥形瓶外,造成V(标准)偏大,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,c(标准)偏大,故D正确;
E.观察读数时,滴定前仰视,滴定后俯视,造成V(标准)偏小,根据c(待测)=$\frac{c(标准)×V(标准)}{V(待测)}$分析,c(标准)偏小,故E错误;
故选ACD.
点评 本题主要考查了中和滴定操作、误差分析以及计算,难度不大,根据课本知识即可完成.

 阅读快车系列答案
阅读快车系列答案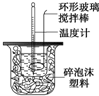 某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在上图装置中进行中和反应.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:
某实验小组设计用50mL 1.0mol/L盐酸跟50mL 1.1mol/L氢氧化钠溶液在上图装置中进行中和反应.在大烧杯底部垫泡沫塑料(或纸条),使放入的小烧杯杯口与大烧杯杯口相平.然后再在大、小烧杯之间填满碎泡沫塑料(或纸条),大烧杯上用泡沫塑料板(或硬纸板)作盖板,在板中间开两个小孔,正好使温度计和环形玻璃搅拌棒通过.通过测定反应过程中所放出的热量可计算中和热.试回答下列问题:(1)环形玻璃搅拌棒的作用是使溶液上下混合均匀,保证溶液上下的温度达到一致.
(2)本实验中用稍过量的NaOH的原因教材中说是为保证盐酸完全被中和.试问:盐酸在反应中若因为有放热现象,而造成少量盐酸在反应中挥发,则测得的中和热偏小(填“偏大”“偏小”或“不变”).
(3)该实验小组做了三次实验,每次取溶液各50mL,并记录如下原始数据.?
| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | 温差(t2-t1)/℃ | ||
| 盐酸 | NaOH溶液 | 平均值 | |||
| 1 | 25.1 | 24.9 | 25.0 | 31.6 | 6.6 |
| 2 | 25.1 | 25.1 | 25.1 | 30.6 | 5.5 |
| 3 | 25.1 | 25.1 | 25.1 | 31.9 | 6.8 |
(4)若用等浓度的醋酸与NaOH溶液反应,则测得的中和热会偏大(填“偏大”“偏小”或“不变”),其原因是用醋酸代替盐酸,醋酸电离要吸收能量,造成测得的中和热数值偏小,但中和热为负值,所以中和热偏大.?
| A. | 食醋除水垢 | B. | 硅胶作干燥剂 | ||
| C. | 漂白粉漂白织物 | D. | 铁粉作食品袋内的脱氧剂 |
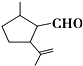 有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )
有机物A是一种重要的化工原料,其结构简式如图,下列检验A中官能团的试剂和顺序正确的是( )| A. | 先加KMnO4酸性溶液,再加银氨溶液,微热 | |
| B. | 先加溴水,再加KMnO4酸性溶液 | |
| C. | 先加银氨溶液,微热,再加溴水 | |
| D. | 先加入足量的新制Cu(OH)2悬浊液,微热,酸化后再加溴水 |
| A. | 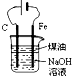 制备 Fe(OH)2 并能较 长时间观察其颜色 | |
| B. | 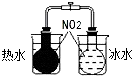 探究温度对平衡移动的影响 | |
| C. | 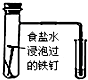 验证铁发生析氢腐蚀 | |
| D. | 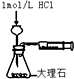 测定反应速率 |
| A. | 氨水 | B. | 氢氧化钡 | C. | 纯碱 | D. | 碳酸钡 |
