题目内容
5.如图1,某校课外活动小组同学设计实验,探究木炭与浓硫酸在加热条件下反应生成气体的成分.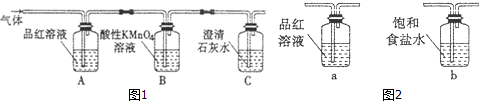
【实验探究】
(1)木炭与浓硫酸反应的化学方程式:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,其中浓H2SO4所起的作用是氧化剂(填“氧化剂”或“还原剂”).若有0.2mol碳的完全反应,则消耗H2S04的质量是39.2g,标况下产生SO2的体积为8.96L.
(2)A装置中品红溶液颜色褪色(填“褪色”或“不褪色”),证明含有SO2(或二氧化硫)气体.
(3)实验过程中,装置C将观察到的现象是石灰水变浑浊.
【实验讨论】
(4)有同学对B装置能否除尽SO2气体有疑义.你认为应该在B、C装置之间连接图2中a装置,以确认S02是否除尽.
【联系实际】
(5)煤和石油的燃烧过程中都有二氧化硫和二氧化碳排放,请提出一条切实可行的减少其排放的措施采周乘坐公共交通工具、骑自行车或步行等方式出行,少用私家车(或节约用水、用电;改善能源结构,开发新能源,如:开发无污染的太阳能、风能、地热能).
分析 (1)根据硫酸中S元素的化合价变化判断浓硫酸的作用;根据反应方程式计算出参加反应的硫酸、二氧化硫的物质的量,再根据m=nM计算出硫酸质量,根据V=nVm计算出标况下二氧化硫的体积;
(2)二氧化硫具有漂白性,能够使品红溶液褪色,据此可以检验二氧化硫;
(3)二氧化碳能够与澄清石灰水反应生成碳酸钙沉淀;
(4)用品红溶液具有是否存在二氧化硫气体;
(5)从减少化石燃料、节约能源等方面考虑可以采取的切实可行的措施.
解答 解:(1)碳与浓硫酸反应的化学方程式为:C+2H2SO4(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+2SO2↑+2H2O,该反应中浓硫酸中硫元素化合价降低被含有,所以浓硫酸在反应中作氧化剂;若有0.2molC完全反应,会消耗0.4mol硫酸,同时生成0.4mol二氧化硫,其中消耗硫酸的质量为:98g/mol×0.4mol=39.2g;生成的二氧化硫在标况下的体积为:22.4L/mol×0.4mol=8.96L,
故答案为:氧化剂;39.2;8.96;
(2)反应中有二氧化硫生成,则图1A装置中品红溶液颜色褪色,证明了混合气体中含有SO2,
故答案为:褪色; SO2(或二氧化硫);
(3)反应生成的混合气体中含有二氧化碳,二氧化碳与氢氧化钙反应生成碳酸钙沉淀,所以装置C中的澄清石灰水变浑浊,
故答案为:石灰水变浑浊;
(4)二氧化硫能够使品红溶液褪色,应该在B、C装置之间连接乙中的a-品红溶液,用于检验二氧化硫气体是否除尽,
故答案为:a;
(5)体现低碳理念的事例有:①采周乘坐公共交通工具、骑自行车或步行等方式出行,②少用私家车或节约用水、用电,③改善能源结构,开发新能源(开发无污染的太阳能、风能、地热能),
故答案为:采周乘坐公共交通工具、骑自行车或步行等方式出行,少用私家车(或节约用水、用电;改善能源结构,开发新能源,如:开发无污染的太阳能、风能、地热能).
点评 本题考查了性质实验方案的设计方法、二氧化硫的化学性质,题目难度中等,明确浓硫酸与碳的反应原理及二氧化硫、二氧化碳的检验方法为解答关键,注意检验二氧化碳时,必须排除二氧化硫的干扰,为易错点,试题培养了学生的分析能力及化学实验能力.

| A. | 易液化 | B. | 极易溶于水 | C. | 水溶液显碱性 | D. | 有刺激性气味 |
①不溶于水的盐(CaCO3、BaSO4等)都是弱电解质
②可溶于水的盐都是强电解质
③0.5mol•L-1所有一元酸溶液中氢离子浓度都是0.5mol•L-1
④强酸溶液中氢离子浓度一定大于弱酸溶液中氢离子浓度
⑤电解质溶液导电的原因是溶液中有自由移动的阴、阳离子
⑥熔融的电解质都能导电.
| A. | ①③⑤⑥ | B. | ②④⑤⑥ | C. | 只有⑤ | D. | 只有⑥ |
| A. | 是直链烃,但分子中3个碳原子不在一条直线上 | |
| B. | 在光照条件下能够与氯气发生取代反应 | |
| C. | 丙烷比丁烷易液化 | |
| D. | 1 mol丙烷完全燃烧消耗5 mol O2 |
| A. | HCl的酸性比HBr强 | |
| B. | 次氯酸的氧化性比次溴酸强 | |
| C. | 氯化氢比溴化氢的热稳定性好 | |
| D. | 氯原子最外层电子数比溴原子最外层电子数多 |
 B是化学实验室中最常见的有机物,其产量可以用来衡量一个国家的石油化工发展水平,还是一种植物生长调节剂.并能进行如图所示的反应.且D能发生加聚反应.
B是化学实验室中最常见的有机物,其产量可以用来衡量一个国家的石油化工发展水平,还是一种植物生长调节剂.并能进行如图所示的反应.且D能发生加聚反应. .
.