题目内容
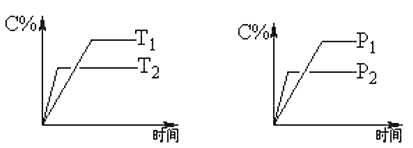
【题目】可逆反应:mA(固)+nB(气)![]() eC(气)+fD(气),反应过程中,当其他条件不变时,C的体积分数(C%)与温度T和压强P的关系如图。下列叙述正确的是
eC(气)+fD(气),反应过程中,当其他条件不变时,C的体积分数(C%)与温度T和压强P的关系如图。下列叙述正确的是
A.达到平衡后,加入催化剂C%增大
B.达到平衡后,若升温平衡向左移
C.m+n<e+f
D.达平衡后,若降压平衡向左移动
【答案】B
【解析】
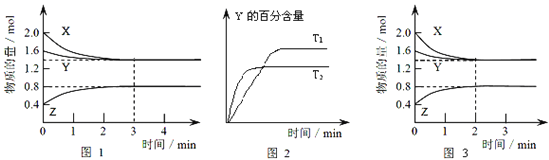
可逆反应,当其他条件一定时,温度越高,反应速率越大,达到平衡所用的时间越短,由图象(1)可知T2>T1,温度越高,平衡时C的体积分数φ(C)越小,故此反应的正反应为放热反应;当其他条件一定时,压强越高,反应速率越大,达到平衡所用的时间越短.由图(2)可知p2>p1,压强越大,平衡时C的体积分数φ(C)越小,可知正反应为气体物质的量增大的反应,即n<e+f,据此结合外界条件对化学平衡的影响分析解答。
A.催化剂只改变化学反应速率,对平衡移动没有影响,C的质量分数不变,故A错误;
B.由上述分析可知,可逆反应mA(固)+nB(气)![]() eC(气)+fD(气)正反应为放热反应,升高温度平衡向吸热方向移动,即向逆反应方向移动,故B正确;
eC(气)+fD(气)正反应为放热反应,升高温度平衡向吸热方向移动,即向逆反应方向移动,故B正确;
C.由上述分析可知,可逆反应mA(固)+nB(气)![]() eC(气)+fD(气)正反应为气体物质的量增大的反应,即n<e+f,故C错误;
eC(气)+fD(气)正反应为气体物质的量增大的反应,即n<e+f,故C错误;
D.达平衡后,若降压平衡向气体体积增大的方向移动,则平衡向右移动,故D错误;
答案选B。

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
【题目】在如图所示装置中,观察到电流计指针偏转,M棒变粗,N棒变细,其中P为电解质溶液。由此判断M、N、P所代表的物质可能是( )

选项 | M | N | P |
A | 锌 | 铜 | 稀硫酸 |
B | 铜 | 锌 | 稀硫酸 |
C | 银 | 锌 | AgNO3溶液 |
D | 铜 | 铁 |
|
A.AB.BC.CD.D