题目内容
【题目】在300mL的密闭固定容器中,一定条件下发生Ni(s)+4CO(g) ![]() Ni(CO)4(g)的反应,该反应平衡常数(K)与温度(T)的关系如下表所示:
Ni(CO)4(g)的反应,该反应平衡常数(K)与温度(T)的关系如下表所示:
T/℃ | 25 | 80 | 230 |
K | 5×104 | 2 | 1.9×10﹣5 |
下列说法不正确的是( )。
A.上述生成Ni(CO)4(g)的反应为放热反应
B.230℃时,该反应的正反应为不自发的反应
C.80℃达到平衡时,测得n(CO)=0.3mol,则Ni(CO)4的平衡浓度为2 mol·L-1
D.25℃时反应Ni(CO)4(g) ![]() Ni(s)+4CO(g)的平衡常数为2×10-5
Ni(s)+4CO(g)的平衡常数为2×10-5
【答案】B
【解析】
A.图表数据分析,平衡常数随温度升高减小,说明平衡逆向进行,逆向是吸热反应,正向是放热反应,故A正确;
B.230℃时,该反应的平衡常数K=1.9×10﹣5,只是说明正反应进行的程度低,但仍为自发的反应,故B错误;
C.80℃达到平衡时,测得n(CO)=0.3mol,c(CO)=![]() =1mol/L,依据平衡常数计算式,K=
=1mol/L,依据平衡常数计算式,K=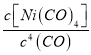 =2,则Ni(CO)4的平衡浓度为2mol/L,故C正确;
=2,则Ni(CO)4的平衡浓度为2mol/L,故C正确;
D.25℃时反应Ni(CO)4(g)![]() Ni(s)+4CO(g)的平衡常数为Ni(s)+4CO(g)
Ni(s)+4CO(g)的平衡常数为Ni(s)+4CO(g)![]() Ni(CO)4(g),平衡常数的倒数═
Ni(CO)4(g),平衡常数的倒数═![]() =2×10-5,故D 正确;
=2×10-5,故D 正确;
故答案为B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目