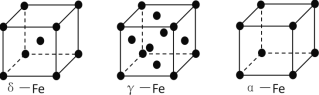
��Ŀ����
����Ŀ������Ԫ��W��X��Y��Z��ԭ�������������ӣ��Ҿ�������20��W��X��Z������֮��Ϊ10��Y��ԭ�Ӱ뾶��ͬ��������Ԫ������С��W��Z�γɵĻ����ﳣ���¿��뱥��NaCl��Һ��Ӧ�����������峣�����и�ͺ��ӽ���������˵���������

A. X�ĵ��������ཫ̫����ת��Ϊ���ܵij��ò���
B. YԪ�ؿ����γɶ��ֺ�����
C. XԪ������Ȼ����ֻ�л���̬û������̬
D. W��Z�γɵĻ������뱥��NaCl��Һ�ķ�ӦҪѡ������ͼװ��
���𰸡�D
��������
����Ԫ��W��X��Y��Z��ԭ�������������ӣ��Ҿ�������20��W��Z�γɵĻ����ﳣ���¿��뱥��NaCl��Һ��Ӧ�����������峣�����и�ͺ��ӽ�����������Ϊ��Ȳ����WΪCԪ�أ�ZΪCaԪ�أ�W��X��Z������֮��Ϊ10����X��������=10-4-2=4��λ�ڢ�A�壬��XΪSiԪ�أ�Y��ԭ�Ӱ뾶��ͬ��������Ԫ������С��Y��ԭ����������Si��λ�ڵ������ڣ�ΪClԪ�أ��ݴ˽��
���ݷ�����֪��WΪCԪ�أ�XΪSi��YΪCl��ZΪCaԪ�ء�
A.����SiΪ���õİ뵼����ϣ������ཫ̫����ת��Ϊ���ܵij��ò��ϣ�A��ȷ��
B.ClԪ�غ��ж��ֻ��ϼۣ������γɶ��ֺ����ᣬ������ᡢ���ᡢ������ȣ�B��ȷ��
C.SiΪ����Ԫ�أ�����Ȼ����ֻ�Ի���̬���ڣ�û������̬��C��ȷ��
D.̼���Ƽ�����ˮ��Ӧ������������ˮ�Ŀ�״���壬������ͼʾװ����ȡ��Ȳ��D����
�ʺ���ѡ����D��

 �»����ܶ�Ա��ϵ�д�
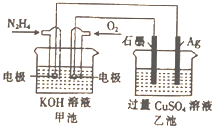
�»����ܶ�Ա��ϵ�д� ����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�
����ͼ����ּ��������ҵ֣�ݴ�ѧ������ϵ�д�����Ŀ����300mL���ܱչ̶������У�һ�������·���Ni(s)+4CO(g) ![]() Ni(CO)4(g)�ķ�Ӧ���÷�Ӧƽ�ⳣ����K�����¶ȣ�T���Ĺ�ϵ���±���ʾ��
Ni(CO)4(g)�ķ�Ӧ���÷�Ӧƽ�ⳣ����K�����¶ȣ�T���Ĺ�ϵ���±���ʾ��
T/�� | 25 | 80 | 230 |
K | 5��104 | 2 | 1.9��10��5 |
����˵������ȷ���ǣ� ����
A.��������Ni(CO)4(g)�ķ�ӦΪ���ȷ�Ӧ
B.230��ʱ���÷�Ӧ������ӦΪ���Է��ķ�Ӧ
C.80��ﵽƽ��ʱ�����n(CO)=0.3mol����Ni(CO)4��ƽ��Ũ��Ϊ2 mol��L��1
D.25��ʱ��ӦNi(CO)4(g) ![]() Ni(s)+4CO(g)��ƽ�ⳣ��Ϊ2��10-5
Ni(s)+4CO(g)��ƽ�ⳣ��Ϊ2��10-5
����Ŀ��25��ʱ���������ʵĵ���ƽ�ⳣ�������ʾ��
��ѧʽ |
|
| HClO |
|
|
����ƽ�ⳣ�� |
|
|
|
|
|
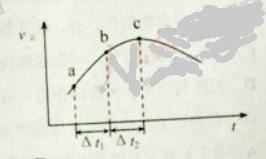
��1��25��ʱ����Ũ�ȵ�![]() ��Һ��
��Һ��![]() ��Һ��
��Һ��![]() ��Һ��3����Һ��pH�ɴ�С��˳��Ϊ________��
��Һ��3����Һ��pH�ɴ�С��˳��Ϊ________��
��2����ҵ�Ͽ��ð�ˮ��ȥβ��![]() ����
����![]() ͨ�백ˮ�У���
ͨ�백ˮ�У���![]() ����
����![]() _____��
_____��
��3�������£���![]() ��Һ�ζ�
��Һ�ζ�![]() ��Һ���õζ�������ͼ��
��Һ���õζ�������ͼ��
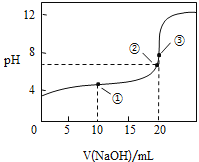
��������ʵ������У�����Ҫ����������Ʒ�� ______������ţ���
![]() ����ƿ b ��ƿc �ζ��ܼ�d ©��e ������f �ζ���
����ƿ b ��ƿc �ζ��ܼ�d ©��e ������f �ζ���
�ڵ���ζ��յ�ı�־�� _____________ ��
�����в����ᵼ�²ⶨ���ƫ�ߵ��� ______ ��
A ��ʽ�ζ�����װҺǰδ�ñ�NaOH��Һ��ϴ
B �ζ������У���ƿҡ����̫���ң���ƿ����Һ�ν���
C ��ʽ�ζ��ܼ��첿���ڵζ�ǰû�����ݣ��ζ��յ�ʱ��������
D �ﵽ�ζ��յ�ʱ�����Ӷ���
����ͼ�����ʾ��Һ��![]() __________
__________![]() ������������������=������ͬ�������ʾ��Һ�У�
������������������=������ͬ�������ʾ��Һ�У�![]() ________
________![]() �������ʾ��Һ����������Ũ���ɴ�С��˳��Ϊ��_________��
�������ʾ��Һ����������Ũ���ɴ�С��˳��Ϊ��_________��