题目内容
11.下列各组离子在指定溶液中,能大量共存的是( )①无色溶液中:K+、Cl-、Ca2+、SO42-、NO3-
②pH=11的溶液中:Na+、AlO2-、NO3-、S2-、SO32-
③水电离的H+浓度c(H+)=10-12mol•L-1的溶液中:Cl-、NO3-、NH4+、SO32-
④加入Mg能放出H2的溶液中:Mg2+、NH4+、Cl-、K+、SO42-
⑤使石蕊变红的溶液中:Fe2+、MnO4-、NO3-、Na+、SO42-
⑥中性溶液中:Fe3+、Al3+、NO3-、Cl-、S2-.
| A. | ①②⑤ | B. | ①③⑥ | C. | ②④ | D. | ①②④ |
分析 ①Ca2+与硫酸根离子反应生成沉淀;
②pH=11的溶液呈碱性,四种离子之间不发生反应,都不与氢氧根离子反应;
③水电离的H+浓度c(H+)=10-12mol•L-1的溶液,水的电离被抑制,溶液可能呈酸性或碱性,铵根离子与氢氧根离子反应,亚硫酸根离子与氢离子反应;
④加入Mg能放出H2的溶液呈酸性,四种离子之间不发生反应,都不与氢离子反应;
⑤使石蕊变红的溶液呈酸性,在酸性条件下硝酸根离子、高锰酸根离子能够氧化亚铁离子;
⑥Fe3+、Al3+都与S2?离子反应.
解答 解:①Ca2+与SO42?反应生成沉淀而不能大量共存,故①错误;
②pH=11的溶液呈碱性,在碱性条件下Na+、AlO2-、NO3-、S2-、SO32-离子之间不发生任何反应,可大量共存,故②正确;
③水电离的H+浓度c(H+)=10-12mol•L-1的溶液,水的电离被抑制,溶液可能呈酸性或碱性,酸性条件下SO32-与NO3-发生氧化还原反应,碱性条件下NH4+不能大量存在,故③错误;
④加入Mg能放出H2的溶液呈酸性,在酸性条件下Mg2+、NH4+、Cl-、K+、SO42-离子之间不发生任何反应,可大量共存,故④正确;
⑤使石蕊变红的溶液呈酸性,在酸性条件下Fe2+与MnO4-、NO3-发生氧化还原反应而不能大量共存,故⑤错误;
⑥Fe3+、S2?离子之间发生氧化还原反应,S2?、Al3+发生双水解反应,在溶液中不能大量共存,故⑥错误;
根据分析可知,能够大量共存的为:②④,
故选C.
点评 本题考查离子共存的正误判断,为中等难度的试题,注意明确离子不能大量共存的一般情况,如:能发生复分解反应的离子之间,能发生氧化还原反应的离子之间等;解决离子共存问题时还应该注意题目所隐含的条件,如:溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;溶液的具体反应条件,如“氧化还原反应”、“加入镁粉产生氢气”等,试题有利于培养学生灵活运用基础知识解决实际问题的能力.

| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
①在点燃H2、CO、CH4等易燃性气体前,必须检验气体的纯度.
②在稀释浓硫酸时,应将浓硫酸沿器壁慢慢注入水中,并用玻璃棒搅拌.
③浓碱对皮肤有腐蚀作用,如不慎沾到皮肤上,应用较多的水冲洗,再涂上硼酸溶液.
④给试管中的液体加热时,液体不超过试管容积的$\frac{1}{3}$
⑤点燃添满酒精的酒精灯.
| A. | 仅①② | B. | 仅①②③ | C. | 仅①②③④ | D. | 全部 |
| A. | A的相对分子质量比B的大16 | |
| B. | 该酯分子结构中一定存在双键 | |
| C. | B的相对分子质量比A大14 | |
| D. | 酯、A、B 3种分子中都含有一种相对分子质量大于60的相同基团 |
| A. | 高分子的结构是长链状的 | |
| B. | 高分子间相互作用的分子间力较强 | |
| C. | 高分子化合物链里的原子是以共价键结合的 | |
| D. | 高分子链之间发生了缠绕 |
| A. | 平衡时甲、乙中Z的体积分数甲>乙 | |
| B. | 平衡时甲中X的转化率为75% | |
| C. | 达到平衡后,再向乙中加入0.25molX,0.75molY和1.5molZ,平衡向生成x的方向移动 | |
| D. | 乙中反应的热化学方程式:2Z(g)═X(g)+3Y(g)△H=+Q2kJ•mol-1 |
| A. | H2O | B. | BF3 | C. | COCl2 | D. | SF6 |
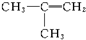 属于同类(“同类”或“不同类”)物质,分子式为C4H8,二者属于碳链异构体.
属于同类(“同类”或“不同类”)物质,分子式为C4H8,二者属于碳链异构体.