题目内容
【题目】已知28 g CuO和MgO的固体混合物与200 mL某H2SO4溶液恰好完全反应,将反应后的溶液小心蒸干,得到固体68 g。则原H2SO4溶液的物质的量浓度和原固体混合物中氧元素的质量分数分别是( )
A.2.5 mol·L-1 28.57%B.2.2 mol·L-1 23.07%
C.1.5 mol·L-1 24.55%D.2.5 mol·L-1 18.37%
【答案】A
【解析】
由题意知,CuO和MgO与H2SO4反应后,转化为CuSO4和MgSO4
CuO——CuSO4 固体质量由80g变为160g,质量增加80g;
MgO——MgSO4 固体质量由40g变为120g,质量增加80g;
质量发生变化的原因是:O——SO4 m
16g 96g 80g
8g 48g 68g-28g=40g
c(H2SO4)=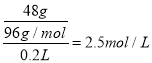 w(O)=
w(O)=![]()
故答案为A。

练习册系列答案
相关题目