题目内容
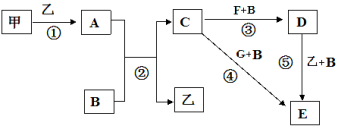
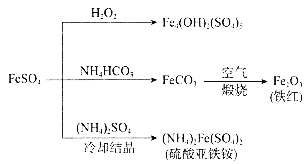
【题目】硫酸亚铁的用途广泛,可以制备下图所示物质,下列说法错误的是( )
A.![]() 属于碱式盐,可用作净水剂
属于碱式盐,可用作净水剂
B.与足量![]() 反应的离子方程式为:
反应的离子方程式为:![]()
C.可用稀硫酸和![]() 溶液检验铁红中是否含有
溶液检验铁红中是否含有![]()
D.“冷却结晶”后的操作是过滤,“煅烧”操作的主要仪器有酒精灯、蒸发皿、玻璃棒
【答案】BD
【解析】
A.Fe4(OH)2(SO4)5电离后的阴离子为OH-和SO42-,阳离子为Fe3+,属于碱式盐,其中Fe3+可水解产生Fe(OH)3的胶体,吸附水中的杂质,可作净水剂,A选项正确;
B.FeSO4与足量NH4HCO3反应的离子方程式为:Fe2++2HCO3-===FeCO3+CO2↑+H2O,B选项错误;
C.Fe2+能使K3[Fe(CN)6]生成蓝色沉淀,用稀硫酸和K3[Fe(CN)6]溶液检验铁红中是否含有FeCO3,若含有,溶液会生成蓝色沉淀,若不含有,则无明显现象,C选项正确;
D.“冷却结晶”后的操作是过滤,“煅烧”操作的主要仪器有酒精灯、三脚架、坩埚、泥三角、玻璃棒,D选项错误;
答案选BD。

【题目】钠和钾是极活泼的金属元素,钠和钾及化合物在生产和生活中有广泛的应用。
(1)写出两种可以食用的含钠化合物的化学式:________。将0.01 mol下列物质(①Na2O2;②Na2O;③Na2CO3;④NaCl)分别加入100 mL蒸馏水中,恢复至室温,所得溶液中阴离子浓度由大到小的顺序是(溶液体积变化忽略不计)_______。
(2)由于钾比钠更活泼,制备K2O一般是用单质钾还原对应的过氧化物、硝酸盐或亚硝酸盐,试写出用钾与硝酸钾反应制取K2O的化学方程式(还有一种单质生成):______________________。K2O2也有强氧化性,试写出其与SO2发生反应的化学方程式:_______________________。
(3)某学生用Na2CO3和 KHCO3组成的某混合物进行实验,测得如表数据(盐酸的物质的量浓度相等且不考虑HCl的挥发)
实验序号 | ① | ② | ③ | ④ |
盐酸体积/mL | 50 | 50 | 50 | 50 |
固体质量/g | 3.06 | 6.12 | 9.18 | 12.24 |
生成气体体积/L(标况) | 0.672 | 1.344 | 1.568 | 1.344 |
根据数据计算所用盐酸的物质的量浓度为__________,原混合物样品中n(Na2CO3)∶n(KHCO3)=_________。