题目内容
【题目】下表列出了①~⑥六种元素在周期表中的位置:
族 周期 | ⅠA | 0 | ||||||
1 | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ||||
请按要求回答下列问题。
(1)元素①的元素符号是_____________。
(2)元素②的单质电子式是______________。
(3)元素⑤的原子结构示意图是______________。
(4)这六种元素中,位于第三周期且原子半径最小的是(填元素符号)_______。
(5)这六种元素的最高价氧化物中,属于两性氧化物的元素是(填元素符号)_______。
(6)在盛有水的小烧杯中加入元素③的单质,发生反应的离子方程式为_______________________;向上述反应后的溶液中再加入元素④的单质,发生反应的化学方程式为______________________。
【答案】C ![]()
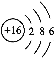 Cl Al 2Na+2H2O=2Na++2OH-+H2↑ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
Cl Al 2Na+2H2O=2Na++2OH-+H2↑ 2Al+2NaOH+2H2O=2NaAlO2+3H2↑
【解析】
根据各元素在周期表中的位置可知,表中各元素分别为:①碳、②氮、③钠、④铝、⑤硫、⑥氯,结合元素原子的结构和性质以及元素周期律知识可对(1)到(6)小题进行解答。
(1)①位于第二周期IVA族的是6号元素碳,元素符号C,答案为:C
(2)元素②的单质是N2,N原子最外层有5个电子,需共用3对电子才能达到8电子饱和结构,所以N2的电子式为:![]() ,答案为:
,答案为:![]()
(3)元素⑤是硫,原子结构示意图为: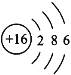 ,答案为:
,答案为:
(4)6种元素中,属第三周期的是钠、铝、硫、氯。同周期元素的原子半径随原子序数的增大而减小,所以它们的原子半径依次减小。答案为:Cl
(5)这六种元素中,铝处于金属和非金属的交界处,其最高价氧化物Al2O3有两性;其他元素最高价氧化物中:CO2、N2O5、SO3、Cl2O7是酸性氧化物,Na2O是碱性氧化物。答案为:Al
(6)钠能与水反应产生氢气和氢氧化钠:2Na+2H2O=2NaOH+H2↑,离子方程式为:2Na+2H2O=2Na++2OH-+H2↑;铝与氢氧化钠溶液反应生成氢气,化学方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑。答案为:2Na+2H2O=2Na++2OH-+H2↑;2Al+2NaOH+2H2O=2NaAlO2+3H2↑

 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案【题目】正丁醛是一种化工原料。某实验小组利用如图装置合成正丁醛。
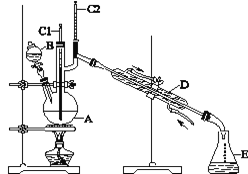
发生的反应如下:CH3CH2CH2CH2OH![]() CH3CH2CH2CHO,反应物和产物的相关数据列表如下:
CH3CH2CH2CHO,反应物和产物的相关数据列表如下:
沸点/℃ | 密度/(g·cm-3) | 水中溶解性 | |
正丁醇 | 117.2 | 0.810 9 | 微溶 |
正丁醛 | 75.7 | 0.801 7 | 微溶 |
实验步骤如下:将6.0 g Na2Cr2O7放入100 mL烧杯中,加30 mL水溶解,与5 mL浓硫酸形成混合溶液,将所得溶液小心转移至B中。在A中加入4.0 g正丁醇和几粒沸石,加热。当有蒸气出现时,开始滴加B中溶液。滴加过程中保持反应温度为90~95 ℃,在E中收集90 ℃以下的馏分。将馏出物倒入分液漏斗中,分去水层,有机层干燥后蒸馏,收集75~77 ℃馏分,产量2.0 g。回答下列问题:
(1)实验中,Na2Cr2O7溶液和浓硫酸添加的顺序为_______。
(2)加入沸石的作用是_____________。若加热后发现未加沸石,应采取的正确方法是__________。
(3)上述装置图中,D仪器的名称是________,E仪器的名称是________。
(4)分液漏斗使用前必须进行的操作是________。
(5)将正丁醛粗产品置于分液漏斗中分水时,正丁醛在_______层(填“上”或“下”)。
(6)反应温度应保持在90~95 ℃,其原因是___________。
(7)本实验中,正丁醛的产率为________%(结果保留两位小数)。