题目内容
2.高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂,下列反应可制取K2FeO4:2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6KCl+8H2O.对于该反应,下列说法正确的是( )| A. | 该反应是置换反应 | |
| B. | 该反应只有K2FeO4为氧化产物 | |
| C. | 3mol氯气参与反应转移电子数为6个 | |
| D. | 该反应条件下K2FeO4的氧化性大于Cl2 |
分析 2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6KCl+8H2O中,Fe元素的化合价由+3价升高为+6价,Cl元素的化合价由0降低为-1价,以此来解答.
解答 解:A.生成物中没有单质,不符合置换反应的特点,故A不选;
B.Fe元素的化合价升高,失去电子被氧化,则氧化产物为K2FeO4,故B选;
C.3mol氯气参与反应转移电子数为3mol×2×(1-0)×NA=6NA,故C不选;
D.氧化剂的氧化性大于氧化产物的氧化性,则反应条件下K2FeO4的氧化性小于Cl2,故D不选;
故选B.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
相关题目
13.下列配合物的配位数不是6的是( )
| A. | K2[Co(NCS)3]Cl | B. | Na2[SiF2Cl2Br2] | C. | Na3[AlF6] | D. | [Cr(NH3)4(H2O)2]Cl3 |
10.100g浓度为18mol/L密度为ρg/mL的浓硫酸中加入一定的水稀释成9mol/L的硫酸,则加入水的体积为( )
| A. | 小于100mL | B. | 等于100mL | C. | 大于100mL | D. | 等于100/ρmL |
17.下列物质分子中有最多原子在一条直线上的是( )
| A. | 乙醇 | B. | 乙烯 | C. | 乙烷 | D. | 苯 |
7.在碱性溶液中,能大量共存的离子组是( )
| A. | Mg2+?SO42-?K+?Cl- | B. | K+?Cl-?NO-3?Cu2+ | ||
| C. | Na+?SO2-4?H+?NO-3 | D. | K+?CO32-?Cl-?Na+ |
14.电解100mL含c(H+)=0.30mol/L的下列各溶液,当电路中通过0.04mol电子时,理论上获得的阴极产物物质的量最大的是( )
| A. | 0.20 mol/L Ag+ | B. | 0.20 mol/L Al3+ | C. | 0.20 mol/L Cu2+ | D. | 0.20 mol/L Mg2+ |
11.已知16S和34Se位于同一主族,下列说法正确的是( )
| A. | 热稳定性:H2Se>H2S>H2O | B. | 原子半径:Se>Cl>S | ||
| C. | 酸性:H2SeO4<H2SO4<HClO4 | D. | 还原性:S2->Se2->Br- |
12.如图是硫酸试剂瓶标签上的部分内容.据此下列说法中,正确的是( )
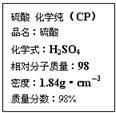

| A. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL | |
| B. | 1 mol Zn与足量的该硫酸反应产生2 g H2 | |
| C. | 该硫酸可以用来干燥硫化氢气体 | |
| D. | 若不小心将该硫酸溅到皮肤上,应立即用NaOH溶液冲洗 |
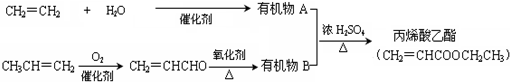
 ,反应类型是加聚反应.
,反应类型是加聚反应.