题目内容
1.下列离子方程式不正确的是( )| A. | 用过量的氨水吸收二氧化硫:2NH3•H2O+SO2═2NH4++SO${\;}_{3}^{2-}$?+H2O | |
| B. | Al(OH)3沉淀中滴加盐酸 Al(OH)3+3H+═Al3++3H2O | |
| C. | AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | 碳酸氢钠溶液中滴加氢氧化钠:HCO3-+OH-═CO32-+H2O |
分析 A.氨水过量生成亚硫酸铵;
B.Al(OH)3沉淀中滴加盐酸,反应生成氯化铝和水;
C.不符合反应客观事实;
D,二者反应生成碳酸钠和水.
解答 解:A.氨水过量生成亚硫酸铵,离子方程式:2NH3•H2O+SO2═2NH4++SO32-+H2O,故A正确;
B.Al(OH)3沉淀中滴加盐酸,离子方程式:Al(OH)3+3H+═Al3++3H2O,故B正确;
C.AlCl3溶液中加入过量氨水,生成氢氧化铝和氯化铵,离子方程式:Al3++3NH3•H2O=Al(OH)3↓+3NH4+,故C错误;
D.碳酸氢钠溶液中滴加氢氧化钠,离子方程式:HCO3-+OH-═CO32-+H2O,故D正确;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意反应物用量对反应的影响,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
11.科学家发现,不管化学反应是一步完成还是分几步完成,该反应的热效应是相同的.已知在25℃,105 Pa时,1mol石墨和1mol一氧化碳完全燃烧生成二氧化碳时的放热分别 是△H=-393.5kJ/mol和△H=-283kJ/mol,下列说法或方程式正确的是( )
| A. | 在相同条件下,C(石墨,s)+CO2(g)═2CO(g),△H=+172.5 kJ/mol | |
| B. | 1mol石墨不完全燃烧,生成CO2和CO混合气体时,放热504.0kJ | |
| C. | 2C(石墨,s)+O2(g)═2CO(g),△H=-110.5kJ/mol | |
| D. | 已知金刚石不如石墨稳定,则石墨转变为金刚石需要放热 |
9.下列叙述中,正确的是( )
| A. | 1 mol H2的质量只有在标准状况下才约为2g | |
| B. | 在标准状况下某气体的体积是22.4L,可认为该气体的物质的量约是1mol | |
| C. | 在20℃时,1mol任何气体的体积总比22.4L大 | |
| D. | 1mol H2和O2的混合气体的质量可能为34g |
6.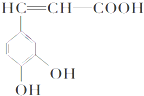 咖啡酸(如图),存在于许多中药,如野胡萝卜、光叶水苏、荞麦等中.咖啡酸有止血作用.下列 关于咖啡酸的说法不正确的是( )
咖啡酸(如图),存在于许多中药,如野胡萝卜、光叶水苏、荞麦等中.咖啡酸有止血作用.下列 关于咖啡酸的说法不正确的是( )
 咖啡酸(如图),存在于许多中药,如野胡萝卜、光叶水苏、荞麦等中.咖啡酸有止血作用.下列 关于咖啡酸的说法不正确的是( )
咖啡酸(如图),存在于许多中药,如野胡萝卜、光叶水苏、荞麦等中.咖啡酸有止血作用.下列 关于咖啡酸的说法不正确的是( )| A. | 咖啡酸的分子式为C9H8O4 | |
| B. | 1 mol咖啡酸可以和含4 molBr2的浓溴水反应 | |
| C. | 1 mol咖啡酸与足量NaHCO3溶液反应能产生标况下约67.2L的CO2 | |
| D. | 不可以用高锰酸钾检验咖啡酸分子中的碳碳双键 |
13.盐酸和KHCO3反应时,能使反应的最初速率明显加快的是( )
| A. | 将盐酸用量增加一倍 | B. | 盐酸的浓度增加一倍,用量减半 | ||
| C. | 温度降低到25度 | D. | 增加KHCO3粉末的量 |
10.现将1mol Cu2S与2mol FeO投入到足量稀硝酸溶液中,充分反应得到Fe(NO3)3、Cu(NO3)2、CuSO4的混合溶液,并产生NO气体.则最终反应所得NO物质的量为( )
| A. | 4mol | B. | 5mol | C. | 6mol | D. | 7mol |
11.在氯水中存在多种分子和离子,它们在不同的反应中表观各自的性质,下列实验观象和结论一致且正确的是( )
| A. | 加入有色布条,一会儿有色布条褪色,说明溶液中有Cl2存在 | |
| B. | 新制氯水可使蓝色石蕊试纸先变红后褪色 | |
| C. | 氯气长时间放置后酸性减弱 | |
| D. | 加入NaOH溶液,氯水黄绿色消失,说明有HClO分子存在 |