题目内容
12.X是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应.(1)若X为氧化物,则X的化学式为Al2O3.
(2)若X为单质,写出其与NaOH溶液反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(3)若X与稀硫酸反应生成无色无味的气体A,与浓氢氧化钠溶液加热反应生成气体B.等物质的量的A和B在水溶液中反应又生成X.常温下X与足量稀氢氧化钠溶液反应的离子方程式为NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
分析 X是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应.
(1)若X为氧化物,则X为氧化铝;
(2)若X为单质,则X为Al,与NaOH溶液反应生成偏铝酸钠与氢气;
(3)若X与稀硫酸反应生成无色无味的气体A,与浓氢氧化钠溶液加热反应生成气体B.等物质的量的A和B在水溶液中反应又生成X,则X为碳酸氢铵,A为二氧化碳、B为氨气.
解答 解:X是中学化学中的常见物质,X既能与稀硫酸反应,又能与氢氧化钠溶液反应.
(1)若X为氧化物,则X为Al2O3,故答案为:Al2O3;
(2)若X为单质,则X为Al,与NaOH溶液反应生成偏铝酸钠与氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(3)若X与稀硫酸反应生成无色无味的气体A,与浓氢氧化钠溶液加热反应生成气体B.等物质的量的A和B在水溶液中反应又生成X,则X为碳酸氢铵,A为二氧化碳、B为氨气,常温下X与足量稀氢氧化钠溶液反应的离子方程式为:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O,故答案为:NH4++HCO3-+2OH-=NH3.H2O+CO32-+H2O.
点评 本题考查无机物推断,注意归纳总结中学常见能与酸、碱反应的物质,难度不大.

练习册系列答案
 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
2.下列实验设计及其对应的离子方程式均正确的是( )
| A. | 用 FeCl3溶液腐蚀铜线路板:Cu+2Fe 3+=Cu2++2Fe2+ | |
| B. | 向沸水中滴加氯化铁溶液制备氢氧化铁胶体:Fe3++3H2O=Fe(OH)3+3H+ | |
| C. | 用惰性电极电解饱和食盐水制备金属钠:2NaCl=2Na+Cl2↑ | |
| D. | 用浓盐酸酸化的 KMnO4溶液与 H2O2反应,证明 H2O2具有还原性:2MnO4-+6H++5H2O2=2Mn2++5O2↑+8H2O |
20.下列物质均有漂白作用,其漂白原理相同的是( )
①二氧化硫
②次氯酸
③过氧化钠
④活性炭
⑤臭氧
⑥过氧化氢.
①二氧化硫
②次氯酸
③过氧化钠
④活性炭
⑤臭氧
⑥过氧化氢.
| A. | ①②⑤⑥ | B. | ①②③④ | C. | ②③⑤⑥ | D. | ①④ |
17.将一定量的铝粉与氧化铜混合加热生成铜和氧化铝,充分反应后,为了检验氧化铜是否完全反应,取反应后的固体,加入足量的稀硫酸中,充分反应后,再将铁片插入溶液中,下列现象,能说明氧化铜没有完全反应的是( )
①加入稀硫酸有气泡产生 ②加入稀硫酸后,没有气泡生成 ③加入稀硫酸后,溶液中有红色不溶物出现 ④插入溶液中铁片表面有红色物质析出.
①加入稀硫酸有气泡产生 ②加入稀硫酸后,没有气泡生成 ③加入稀硫酸后,溶液中有红色不溶物出现 ④插入溶液中铁片表面有红色物质析出.
| A. | 只有②③ | B. | 只有③④ | C. | 只有④ | D. | ①②③④ |
1.下列离子方程式不正确的是( )
| A. | 用过量的氨水吸收二氧化硫:2NH3•H2O+SO2═2NH4++SO${\;}_{3}^{2-}$?+H2O | |
| B. | Al(OH)3沉淀中滴加盐酸 Al(OH)3+3H+═Al3++3H2O | |
| C. | AlCl3溶液中加入过量氨水:Al3++4OH-═AlO2-+2H2O | |
| D. | 碳酸氢钠溶液中滴加氢氧化钠:HCO3-+OH-═CO32-+H2O |
2.下列离子组中,在由水电离出的c(H+)•c(0H-)=1×10-26mol•L-1的溶液中一定能大量共存的是( )
| A. | Na+、Mg2+、Al3+、Cl- | B. | Na+、K+、Cl-、SO42- | ||
| C. | HCO3-、Na+、Cl-、K+ | D. | I-、Fe2+、Na+、NO3- |
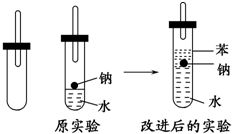 某化学实验小组对钠与水的反应进行了研究,他们设计了如图所示的实验装置.请回答下列问题:
某化学实验小组对钠与水的反应进行了研究,他们设计了如图所示的实验装置.请回答下列问题: