题目内容
13.已知:甲$→_{石墨电极}^{电解}$乙$\stackrel{H_{2}}{→}$丙,若丙的水溶液显酸性,则甲可能为( )| A. | NaCl | B. | KOH | C. | Al2O3 | D. | MgSO4溶液 |
分析 A、用石墨电极电解NaCl溶液时阳极生成氯气,氯气可与氢气反应生成氯化氢;
B、用石墨电极电解KOH溶液时阳极生成氧气,氧气可与氢气反应生成水;
C、用石墨电极电解熔融Al2O3时阳极生成氧气,氧气可与氢气反应生成水;
D、用石墨电极电解MgSO4溶液时阳极生成氧气,氧气可与氢气反应生成水;
解答 解:A、用石墨电极电解NaCl溶液时阳极生成氯气,氯气可与氢气反应生成丙为氯化氢,氯化氢的水溶液显酸性,故A正确;
B、用石墨电极电解KOH溶液时阳极生成氧气,氧气可与氢气反应生成丙为水,所以丙的水溶液不显酸性,故B错误;
C、用石墨电极电解熔融Al2O3时阳极生成氧气,氧气可与氢气反应生成丙为水,所以丙的水溶液不显酸性,故C错误;
D、用石墨电极电解MgSO4溶液时阳极生成氧气,氧气可与氢气反应生成丙为水,所以丙的水溶液不显酸性,故D错误;
故选:A.
点评 本题主要考查了利用电解原理来推断,关键是判断好用石墨电极电解阴阳极的产物,根据丙的水溶液显酸性判断,难度不大.

练习册系列答案
相关题目
3.糖生物电池是一种酶催化燃料电池(EFC),它使用便宜的酶代替贵金属催化剂,利用空气氧化糖类产生电流.下列有关判断不合理的是( )
| A. | 该电池不宜在高温下工作 | |
| B. | 若该电池为酸性介质,正极反应式为:O2+4e-+4H+═2H2O | |
| C. | 放电过程中,电池内阳离子向正极迁移 | |
| D. | 若该电池为碱性介质,以葡萄糖为原料并完全氧化,负极反应式为:C6H12O6-24e-+6H2O═6CO2↑+24H+ |
4.氰氨化钙是一种重要的化工原料,其制备的化学方程式为:CaCO3+2HCN→CaCN2+CO↑+H2↑+CO2↑,下列说法正确的是( )
| A. | CO为氧化产物,H2为还原产物 | B. | CaCN2含有共价键,属于共价化合物 | ||
| C. | HCN既是氧化剂又是还原剂 | D. | 每消耗10g CaCO3生成2.24L CO2 |
1.某一不饱和酯类化合物(如图)在药物、涂料等领域应用广泛,下列有关说法不正确的是( )

| A. | 能使KMnO4溶液褪色 | |
| B. | 1mol的该化合物和足量的钠反应生成1molH2 | |
| C. | 能与溴发生取代反应和加成反应 | |
| D. | 1mol该化合物最多与2molNaOH反应 |
8.下列离子方程式中,正确的是( )
| A. | 向AgCl悬浊液中加入KBr溶液:Ag++Br-=AgBr | |
| B. | 用铁棒作阴极、碳棒作阳极电解饱和氯化镁溶液:2C1-+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2OH- | |
| C. | 向等物质的量浓度的NaOH和Na2CO3的混合溶液中加入稀盐酸:2OH-+CO32-+4H+═CO2↑+3H2O | |
| D. | 在强碱性溶液中NaClO与Fe(OH)3生成Na2FeO4:4OH-+3ClO-+2Fe(OH)3═2FeO43-+3C1-+5H2O |
18.在对电子运动状态的描述中,确定一个“轨道”的方面包括( )
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子的自旋状态.
①电子层 ②电子亚层 ③电子云的伸展方向 ④电子的自旋状态.
| A. | ①②③④ | B. | ①②③ | C. | ①② | D. | ① |
2.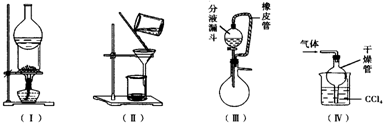 下列实验装置用途正确的是( )
下列实验装置用途正确的是( )
 下列实验装置用途正确的是( )
下列实验装置用途正确的是( )| A. | 装置(Ⅰ)可用于I2与NH4Cl混合物的分离 | |
| B. | 装置(Ⅱ)用于分离Fe(OH)3胶体和FeCl3溶液 | |
| C. | 装置(Ⅲ)橡皮管起到平衡气压,使液体顺利流下的作用 | |
| D. | 装置(Ⅳ)用于吸收HCl或NH3 |
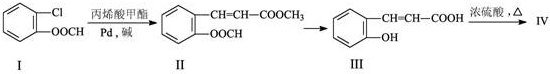
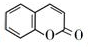
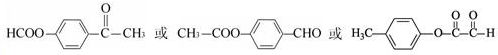
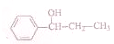 的化学方程式(无机试剂任选)
的化学方程式(无机试剂任选)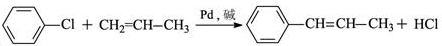 、
、 .
.