题目内容
【题目】25℃时,向纯水中通入Cl2至饱和,再逐滴滴加0.1mol/L的NaOH溶液,实验过程中得到如下图所示的pH变化曲线。下列有关说法正确的是
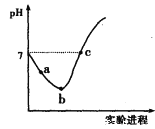
A. pH=7时,一定有c(Na+)=c(Cl-)+c(ClO-)
B. 从a点到b点,Cl2在水中的溶解度增大
C. b点溶液中:c(H+)=c(Cl-)+c(OH-)+c(HClO)
D. 从b点到c点,溶液中![]() 减小
减小
【答案】D
【解析】A、一开始为纯水,溶液中无钠离子,只有在c点pH=7时,c(H+)= c(OH-),根据电荷守恒有:c(Na+)+c(H+)=c(Cl-)+c(ClO-)+c(OH-),则c(Na+)=c(Cl-)+c(ClO-),选项A错误;B、一定温度下,氯气的溶解度不变,选项B错误;C、b点还没加入氢氧化钠,只是氯水,根据电荷守恒有:c(H+)=c(Cl-)+c(OH-)+c(ClO-),选项C错误;D、从b点到c点,逐渐加入氢氧化钠溶液,氢离子浓度降低,平衡Cl2+H2O![]() H++Cl-+HClO正向移动,c(ClO-)增大,故溶液中
H++Cl-+HClO正向移动,c(ClO-)增大,故溶液中![]() 减小,选项D正确。答案选D。
减小,选项D正确。答案选D。

练习册系列答案
相关题目



