题目内容
【题目】下列实验设计能够成功的是 ( )
实验目的 | 实验步骤及现象 | |
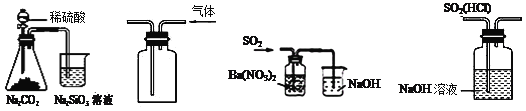
A | 检验亚硫酸钠试样是否变质 | 试样 |
B | 检验某盐是否为铵盐 | 试样 |
C | 证明酸性条件下H2O2氧化性比I2强 | NaI溶液 |
D | 除去氯化钠晶体中少量硝酸钾 | 试样 |
A.AB.BC.CD.D
【答案】D
【解析】
A.亚硫酸钡可被硝酸氧化成硫酸钡,所以即便没有变质,白色沉淀也不溶解,A不合题意;
B.铵盐受热不一定产生氨气,铵盐只有与碱作用时才能产生NH3,B不合题意;
C.稀硝酸也能将I-氧化成I2,不能肯定I-是被H2O2氧化,C不合题意;
D.KNO3的溶解度受温度的影响较大而NaCl的溶解度受温度的影响较小,方案设计合理,D符合题意。
故选D。

 龙人图书快乐假期暑假作业郑州大学出版社系列答案
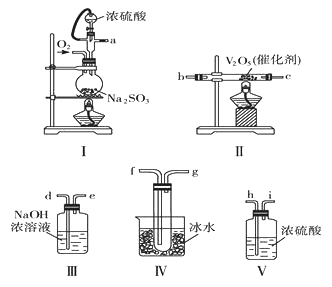
龙人图书快乐假期暑假作业郑州大学出版社系列答案【题目】某化学小组用下列装置和试剂进行实验,探究O2与KI溶液发生反应的条件。
供选试剂:质量分数为30%的H2O2溶液、0.1 mol·L-1的H2SO4溶液、MnO2固体、KMnO4固体。
(1)小组同学设计甲、乙、丙三组实验,记录如下:
操作 | 现象 | |
甲 | 向装置I的锥形瓶中加入MnO2固体,向装置I的____中加入质量分数为30%的H2O2溶液,连接装置I、III,打开活塞 | 装置I中产生无色气体并伴随大量白雾;装置III中有气泡冒出,溶液迅速变蓝 |
乙 | 向装置II中加入KMnO4固体,连接装置II、III,点燃酒精灯 | 装置III中有气泡冒出,溶液不变蓝 |
丙 | 向装置II中加入____,向装置III中再加入适量0.1mol·L-1的H2SO4溶液,连接装置II、III,点燃酒精灯 | 装置III中有气泡冒出,溶液变蓝 |
(2)丙实验中O2与KI溶液反应的离子方程式为___________________________________。
(3)对比乙、丙实验可知,O2与KI溶液发生反应的适宜条件是__________。为进一步探究该条件对反应速率的影响,可采取的实验措施是____________________________。
(4)由甲、乙、丙三组实验推测,甲实验中可能是I中的白雾使溶液变蓝。为了验证推测,可将装置I中产生的气体通入_________(填字母)溶液中,依据实验现象来证明白雾中含有H2O2。
A.酸性KMnO4 B.FeCl2 C.H2S
(5)资料显示:KI溶液在空气中久置的过程中会被缓慢氧化:4KI+O2+2H2O=2I2+4KOH。该小组同学取20 mL久置的KI溶液,向其中加入几滴淀粉溶液,结果没有观察到溶液颜色变蓝,他们猜想可能是发生了反应___________________________________(写离子方程式)造成的,请设计实验证明他们的猜想是否正确:___________________________________。
【题目】如图是某小组设计的用干燥氯气和甲苯合成一氯化苄(C6H5CH2Cl,其中C6H5-表示苯基)并分离产物的实验装置。甲苯及各种氯化苄的物理性质如表所示。
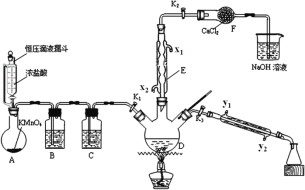
物理性质 | 熔点℃ | 沸点℃ | 密度gcm-3 |
甲苯 | -95 | 110 | 0.86 |
一氯化苄(C6H5CH2Cl) | -45 | 179 | 1.10 |
二氯化苄(C6H5CHCl2) | -17 | 205 | 1.26 |
三氯化苄(C6H5CCl3) | -4.4 | 221 | 1.37 |
回答下列问题:
(1)仪器F的名称是__________;
(2)瓶B和C中盛放的试剂应分别为__________(填序号);
a.蒸馏水;浓硫酸 b.饱和食盐水;浓硫酸
c.浓硫酸;酸性KMnO4溶液 d.饱和NaHCO3溶液;浓硫酸
(3)两处冷凝水的进水口应分别为__________(填序号);
A . x1、y1 B. x1、y2 C. x2、y1 D.x2、y2
(4)在回流反应的过程中,由于温度控制不当,部分产物从K2处被蒸出。取烧杯中的少量吸收液于试管中,滴入新制氢氧化铜悬浊液并加热,观察到有砖红色沉淀生成。则在吸收液中发生反应的化学方程式为______________________;
(5)反应结束后,撤去E、F及尾气吸收装置,插上玻璃塞。保持K1关闭,打开K3,加热三颈烧瓶,分馏出一氯化苄,应选择的温度范围是__________;
(6)由于某同学操作时不慎将含铁的沸石加入三颈烧瓶,在分馏时得到了异常馏分X。用质谱法测得X的相对分子质量与二氯化苄相同,核磁共振氢谱显示X中有3种不同化学环境的氢。已知苯环上存在甲基或氯甲基是,后续取代苯环的基团主要引入其邻位或对位,X的结构简式可能为__________。