题目内容
【题目】已知密闭容器中进行的合成氨反应为N2+3H2![]() 2NH3,该反应为放热反应。下列判断正确的是( )
2NH3,该反应为放热反应。下列判断正确的是( )
A. 1 mol N2和3 mol H2的能量之和与2 mol NH3具有的能量相等
B. 反应过程中同时有1.5 mol H—H键、3 mol N—H键断裂时,N2的浓度维持不变
C. 降低NH3的浓度,正反应速率增大,逆反应速率减小
D. 当反应速率满足v(N2)∶v(H2)=1∶3时,反应达到最大限度
【答案】B
【解析】
A.合成氨反应为放热反应,反应物总能量高于生成物总能量,A项错误;
B.反应过程中有1.5 mol H—H键、3 mol N—H键同时断裂时,正反应速率等于逆反应速率,反应达到平衡,N2的浓度不变,B项正确;
C.降低NH3的浓度,正反应速率不会增大,C项错误;
D.任何时刻,都有各物质表示的化学反应速率之比等于化学计量数之比,均满足v(N2)∶v(H2)=1∶3,不一定是平衡状态,D项错误;
本题答案选B。

 金博士一点全通系列答案
金博士一点全通系列答案【题目】实验室用绿矾(FeSO4·7H2O)为原料制备补血剂甘氨酸亚铁[(H2NCH2COO)2Fe],有关物质性质如下:
甘氨酸(H2NCH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
I.配制含0.10molFeSO4的绿矾溶液。
II.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL1.1mol/LNH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
III.制备(H2NCH2COO)2Fe:实验装置如下图(夹持和加热仪器已省略),将实验II得到的沉淀和含0.20mol甘氨酸的水溶液混合后加入C中,然后利用A中反应产生的气体将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
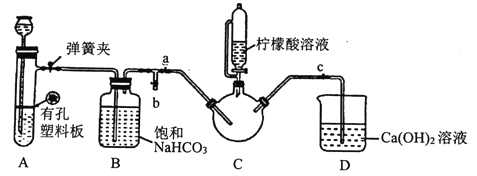
回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为____(写化学式)。
(2)实验II中:生成沉淀的离子方程式为________________。
(3)实验III中:
①检查装置A的气密性的方法是_________。
②装置A中所盛放的药品是_______ (填序号)。
a.Na2CO3和稀H2SO4 b.CaCO3和稀H2SO4 c.CaCO3和稀盐酸
③确认c中空气排尽的实验现象是______________。
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是_______。
⑤洗涤实验III中得到的沉淀,所选用的最佳洗涤试剂是___(填序号)。
a.热水 b.乙醇溶液 c.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为_____。