题目内容
14.在5L物质的量浓度为2mol/l的K2SO4溶液中K+的物质的量浓度为( )| A. | 2mol/l | B. | 4mol/l | C. | 1 mol/l | D. | 20mol/l |
分析 2mol/l的K2SO4溶液中K+的物质的量浓度为定值,与所取的溶液的体积为5L无关,据此分析.
解答 解:根据K2SO4的化学式可知,K+的物质的量浓度为K2SO4的浓度的2倍,与所取的溶液的体积为5L无关,故只要是2mol/L的K2SO4溶液,其钾离子的浓度均为4mo/L,故选B.
点评 本题考查了溶液中离子浓度的求算,应注意的是溶液中离子的浓度与所取的溶液的体积无关,难度不大,但此题的粗错率较高.

练习册系列答案
相关题目
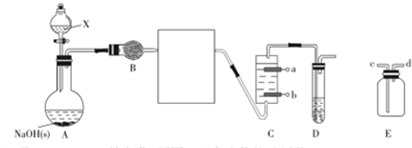
4.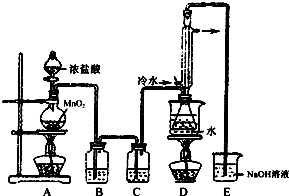 S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的反应原理有两种:
S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的反应原理有两种:
①CS2+3Cl2$\frac{\underline{\;95~100℃\;}}{\;}$CCl4+S2Cl2;
②2S+Cl2$\frac{\underline{\;111~140℃\;}}{\;}$S2Cl2.
已知:S2Cl2易与水反应,S2Cl2+Cl2$\stackrel{△}{?}$2SCl2.
下列是几种物质的熔沸点和反应装置图
(1)利用如图装置(部分夹持仪器已略去)来制备S2Cl2,反应原理是①(填写以上两种反应原理的数字序号).
(2)若装置C更换成干燥管,则装置C中可选用的固体试剂是无水氯化钙或五氧化二磷.
(3)D装置中冷凝管的作用是冷凝回流、导气;反应结束后,将D装置锥形瓶内的混合物中分离出产物的方法是蒸馏.
(4)S2Cl2与足量水反应有黄色沉淀生成,产生的无色气体能使品红溶液褪色,则该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl↑.
(5)为了提高制得的产品S2Cl2的纯度,关键的操作是控制好温度和控制浓盐酸的滴速不能太快.
(6)图中尾部装置不够完善,存在的问题是在D和E之间增加干燥装置,同时尾气吸收要防倒吸.
 S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的反应原理有两种:
S2Cl2是工业上常用的硫化剂,实验室制备S2Cl2的反应原理有两种:①CS2+3Cl2$\frac{\underline{\;95~100℃\;}}{\;}$CCl4+S2Cl2;
②2S+Cl2$\frac{\underline{\;111~140℃\;}}{\;}$S2Cl2.
已知:S2Cl2易与水反应,S2Cl2+Cl2$\stackrel{△}{?}$2SCl2.
下列是几种物质的熔沸点和反应装置图
| 物质 | 沸点/℃ | 熔点/℃ |
| S | 445 | 113 |
| CS2 | 47 | -109 |
| CCl4 | 77 | -23 |
| S2Cl2 | 137 | -77 |
(2)若装置C更换成干燥管,则装置C中可选用的固体试剂是无水氯化钙或五氧化二磷.
(3)D装置中冷凝管的作用是冷凝回流、导气;反应结束后,将D装置锥形瓶内的混合物中分离出产物的方法是蒸馏.
(4)S2Cl2与足量水反应有黄色沉淀生成,产生的无色气体能使品红溶液褪色,则该反应的化学方程式为2S2Cl2+2H2O═3S↓+SO2↑+4HCl↑.
(5)为了提高制得的产品S2Cl2的纯度,关键的操作是控制好温度和控制浓盐酸的滴速不能太快.
(6)图中尾部装置不够完善,存在的问题是在D和E之间增加干燥装置,同时尾气吸收要防倒吸.
2.(1)选择下列某种答案的序号,填入下表的空格
①同位素 ②同素异形体 ③同分异构体 ④同系物 ⑤同种物质
(2)现有下列各化合物:
A.CH3CH2CH2CHO与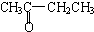 B.
B.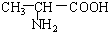 与
与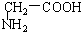 C.
C.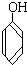 与
与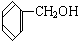
D.CH3CH2C≡CH与CH2═CH-CH=CH2E. 与
与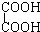 F、戊烯和环戊烷
F、戊烯和环戊烷
①上述化合物中的含氧官能团是(写名称)醛基;羰基;羧基;根据官能团的特点可将C中两化合物划分为酚类和醇类.
②若将A中两化合物看作是某单烯烃被酸性高锰酸钾溶液氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.
①同位素 ②同素异形体 ③同分异构体 ④同系物 ⑤同种物质
| 物质 名称 | 红磷 与白磷 | 庚烷与 十六烷 | 氯仿与 三氯甲烷 | 氕与 氘、氚 | 2--甲基戊烷与 2,3--二甲基丁烷 |
| 相互 关系 |
A.CH3CH2CH2CHO与
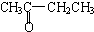 B.
B.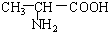 与
与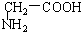 C.
C. 与
与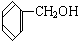
D.CH3CH2C≡CH与CH2═CH-CH=CH2E.
 与
与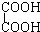 F、戊烯和环戊烷
F、戊烯和环戊烷①上述化合物中的含氧官能团是(写名称)醛基;羰基;羧基;根据官能团的特点可将C中两化合物划分为酚类和醇类.
②若将A中两化合物看作是某单烯烃被酸性高锰酸钾溶液氧化生成的,则该单烯烃的结构简式为CH3CH2CH2CH=C(CH3)CH2CH3.
6.有机物M的结构简式如下:
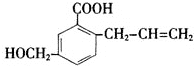
下列有关M的叙述不正确的是( )

下列有关M的叙述不正确的是( )
| A. | M的分子式为C11H1203 | B. | 能使溴的四氯化碳溶液褪色 | ||
| C. | -定条件下,M能生成高分子化合物 | D. | 能发生加成反应不能发生取代反应 |
3.100mL 0.3mol/L Na2SO4溶液和50mL 0.2mol/L Al2(SO4)3溶液混合后,取出该混合后的溶液10mL,则这10mL溶液中SO42-的物质的量浓度为( )
| A. | 0.20 mol/L | B. | 4mol/L | C. | 0.40 mol/L | D. | 6 mol/L |
4.X、Y、Z、W、R是5种短周期元素,其原子序数依次增大.X是周期表中原子半径最小的元素,Y原子最外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等.下列说法正确的是( )
| A. | 元素X与Z、Y 与W形成的化合物都为离子化合物 | |
| B. | 元素X与Y,Z与Y形成的二元化合物都只有一种 | |
| C. | Y、Z、W三种元素形成的离子半径随原子序数的增加而增大 | |
| D. | 元素W、R的最高价氧化物的水化物都是强酸 |
 和
和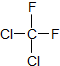 (6)
(6)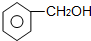 和
和 (7)C2H2和C4H6
(7)C2H2和C4H6 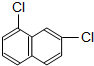 和
和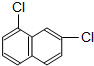 (9)乙醇和乙醚 (10)淀粉和纤维素(11)
(9)乙醇和乙醚 (10)淀粉和纤维素(11)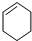 与1-乙炔.
与1-乙炔.