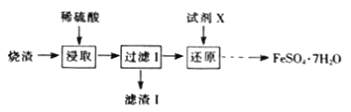
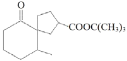
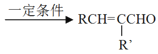
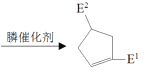
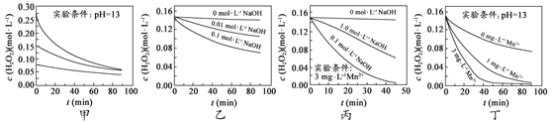
��Ŀ����
����Ŀ���Ʊ�ˮ���£�N2H4��H2O���ķ�Ӧԭ����CO(NH2)2+ 2NaOH + NaClO=Na2CO3+N2H4��H2O+NaCl����֪CO(NH2)2�е㣺133 ����ˮ��������Ҫ����ԭ�ϣ��е㣺118 �����ױ��������밴Ҫ��ش������Ʊ�ˮ����ʵ����й����⡣
��1���Ʊ� NaClO ��Һ��ʵ��װ����ͼ��ʾ��

��ƿ�з�����Ӧ���ӷ���ʽ��__________________________��
��2����ȡˮ���£�ʵ��װ������ͼ��ʾ���г�װ�����ԣ�
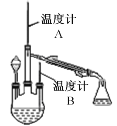
���Ʒ�Ӧ�¶ȣ��ٽ���Һ©������Һ��������������ƿ�У���ַ�Ӧ��������������ƿ�ڵ���Һ���ռ���Ʒ��
����Һ©����ʢװ��ҩƷ��NaOH��Һ��_______________��
����ʢ�ŵ������Ƿ�ֹ___________________________________��
����ʵ���ռ���Ʒ���ʱ�Ĺؼ������ǿ���_______________________________��
��3���ⶨ������µĺ�����
����֪ˮ������һ����������I2��Ӧ����N2����ɸ÷�Ӧԭ���Ļ�ѧ����ʽ��
____N2H4��H2O +____ I2 +6NaHCO3+H2SO4 = ____ N2��+____ NaI +6CO2��+Na2SO4 +7H2O
__________________________
���ⶨʵ��IJ������£�
a����ȡ��� 5.000 g����ˮ���Ƴ�1000 mL����Һ��Һ��
b����ȡ10.00 mL����ƿ�У�����10 mLˮ��ϡ���ᡢ���� NaHCO3���壨��֤�ζ���������Һ�� pH ������ 6.5���ң���2�ε�����Һ��ҡ�ȡ�
c����0.2000 mol/L I2��Һ�ζ�������Һ����___________________________����¼����I2��Һ�������
d��_______________________________��Ȼ�������ݡ�
�������ݴ������ζ�����I2�ı���ҺΪ 8.20 mL�������ˮ���£�N2H4��H2O������������Ϊ____________��
���𰸡�Cl2 +2OH-= ClO-+Cl-+ H2O NaClO��Һ ���ɵ�ˮ���»ᱻδ��Ӧ�Ĵ����������� �¶ȼ�AΪ118 �� 1 2 1 4 ��ɫ�Ұ���Ӳ���ʧ �ظ�����b��c����ʵ�����2~3�� 82.00%
��������
��1����NaOH��Һ��ͨ��Cl2���Ƶ�NaClO�����ӷ���ʽΪ��Cl2+2OH-=ClO-+Cl-+H2O��
��2���ٷ�Һ©����ʢ��NaOH��Һ��NaClO��Һ������NaClOֱ�ӷ���������ƿ�У�NaClO�ɽ���Ӧ���ɵ�ˮ����ֱ��������Ӱ����ʣ�
����Ϊˮ���µķе�Ϊ118��������Ҫ������ϵ�¶���118�����Է�ֹ������������������������¶�Ӧ���¶ȼƵ�ˮ�������������ƿ֧�ܿڳ�����֤����������¶Ⱥ㶨��
��3���������Ļ�ѧ����ʽΪN2H4��H2O+2I2+6NaHCO3+H2SO4=N2��+4NaI+6CO2��+Na2SO4+7H2O��
�ڵ���ϵ��ɫ����ɫ�Ұ�����ڲ���ɫʱ��˵���ζ��ﵽ���յ㣻Ϊ��Сʵ������Ҫ�ظ�ʵ��2-3�Σ�
�۸��ݷ���ʽ��֪��ƿ��![]() =
=![]() =0.041mol/L���ʴ���Һ��c(N2H4��H2O)=0.082mol/L��m(N2H4��H2O)=0.082
=0.041mol/L���ʴ���Һ��c(N2H4��H2O)=0.082mol/L��m(N2H4��H2O)=0.082![]() 50=4.10g���������ˮ���µ���������Ϊ
50=4.10g���������ˮ���µ���������Ϊ![]() =82.00%��
=82.00%��

����Ŀ������ˮ���ᣨ��˾ƥ�֣���Ŀǰ����ҩ��֮һ��ʵ����ͨ��ˮ��������������Ʊ���˾ƥ�ֵ�һ�ַ������£�

ˮ���� | ������ | ����ˮ���� | |
�۵�/�� | 157~159 | -72~-74 | 135~138 |
����ܶ�/��g��cm��3�� | 1.44 | 1.10 | 1.35 |
��Է������� | 138 | 102 | 180 |
ʵ����̣���100 mL��ƿ�м���ˮ����6.9 g��������10 mL�����ҡ��ʹ������ȫ�ܽ⡣�����μ�0.5 mLŨ�������ȣ�ά��ƿ���¶���70 �����ң���ַ�Ӧ�������������²���.
���ڲ��Ͻ����½���Ӧ��Ļ���ﵹ��100 mL��ˮ�У��������壬���ˡ�
�����ýᾧ��Ʒ����50 mL����̼��������Һ���ܽ⡢���ˡ�
����Һ��Ũ�����ữ����ȴ�����˵ù��塣
�ܹ��徭�����ð�ɫ������ˮ���ᾧ��5.4 g��
�ش��������⣺
��1���úϳɷ�Ӧ��Ӧ����__________���ȡ������ţ�
A����ˮԡ B���ƾ��� C��ú���� D����¯
��2�����в��������У�������ʹ�õ���________�����ţ�������ʹ�õ�_______________________�������ƣ���

��3��������ʹ����ˮ��Ŀ����______________________________________��
��4�����б���̼�����Ƶ�������_________________________________���Ա���˳�ȥ�������ʡ�
��5���ܲ��õĴ�������Ϊ____________��
��6����ʵ��IJ�����_________%��