题目内容
【题目】下列图中的实验方案,不能达到相应实验目的是
A.对钢铁闸门防腐保护
B.除去CO2气体中混有的SO2
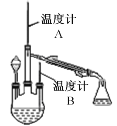
C.验证CH3CH2Br与NaOH乙醇溶液共热产物有乙烯生成
D.验证CuSO4对H2O2分解反应有催化作用
【答案】D
【解析】
A.将闸门与电源负极相连,为外加电源的阴极保护法,可以保护闸门,A正确;
B.NaHCO3可与SO2发生生成CO2,但不与CO2发生反应,可以出去CO2气体中混有的SO2,B正确;
C.将产物通入水中可以将气体中混有的少量溴乙烷冷却液化,再将气体通入酸性高锰酸钾溶液,若变色说明溴乙烷与NaOH反应生成乙烯气体,C正确;
D.验证CuSO4对过氧化氢分解的催化作用,应保证两个实验的温度相同,D错误;
故选D。

练习册系列答案
 文敬图书课时先锋系列答案
文敬图书课时先锋系列答案
相关题目