��Ŀ����
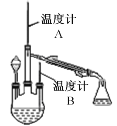
����Ŀ����ҵ�ϲ����������յ�����(��Ҫ�ɷ�ΪFe2O3��SiO2����������������)��ȡ�̷�(FeSO4��7H2O)��������ͼ��
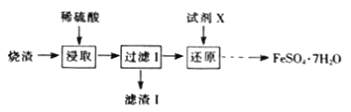
��1�����������Ҫ�ɷ���___(�ѧʽ)��
��2����ԭʱ���Լ�X��ѡ��SO2���䷴Ӧ�����ɵ���������(�ѧʽ)___��
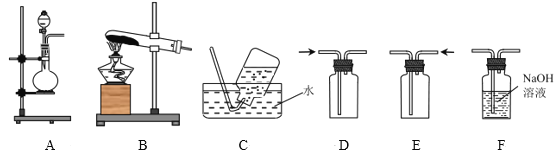
��3���ӻ�ԭ�����Һ�еõ���Ʒ��Ӧ���еIJ�����___��___�����ˡ�ϴ�ӡ����
��4���̷�(FeSO4��7H2O)��ҽѧ�ϳ�������Ѫ����ij����С��ͨ������ʵ�鷽���ⶨij��Ѫ�����������ӵĺ�����
����a��ȡ10Ƭ��Ѫ����Ʒ��ȥ���¡���ĥ���ܽ⡢���ˣ�����Һ���250.00mL��Һ��
����b��ȡ������Һ25.00mL����ƿ�У���������ϡ�����ữ���μ�0.1000mol/L��KMnO4��Һ����ǡ����ȫ��Ӧ����¼���ĵ�KMnO4��Һ�����(�ٶ�ҩƷ�������ɷֲ���KMnO4��Ӧ)�������ķ�ӦΪ��MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O��
����c���ظ�������b��2~3�Σ�ƽ������KMnO4��Һ20.00mL���ò�Ѫ�����������ӵĺ���Ϊ___mg/Ƭ��
���𰸡�SiO2 SO42- ����Ũ�� ��ȴ�ᾧ 56
��������
�������յ�����(��Ҫ�ɷ�ΪFe2O3��SiO2��������������)��������м����������ᣬFe2O3���ᷴӦ���ɵ���������SiO2����Ӧ�����ˣ�������ΪSiO2��
(1) �������յ�����(��Ҫ�ɷ�ΪFe2O3��SiO2��������������)��������м����������ᣬFe2O3���ᷴӦ���ɵ���������SiO2����Ӧ�����ˣ�������ΪSiO2;
(2)����Һ�м���SO2�������ӻ�ԭΪ�������ӣ����ӷ���ʽΪ��2Fe3++ SO2+2H2O= SO42-+ 2Fe2++4H+,�����䷴Ӧ�����ɵ���������SO42-��
(3)�ӻ�ԭ�����Һ�еõ���Ʒ��Ӧ���еIJ���������Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ����(4)�ɷ�ӦMnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O��֪���ڹ�ϵ��MnO4-��5Fe2+������ƽ������0.1000mol/L ��KMnO4��Һ20.00mL����������ĵ�KMnO4�����ʵ���Ϊ�� 0.1000mol/L��20��10-3L=0.002mol���������ĵ�Fe2+�����ʵ���Ϊ��0.002mol��5=0.01mol���ʸò�Ѫ����ÿƬ���������ӵĺ���Ϊ��(0.01mol ��56g/mol)/10=0.056g=56mg��