题目内容
【题目】室温时,向20mL![]() 的醋酸溶液中不断滴入
的醋酸溶液中不断滴入![]() 的NaOH溶液,溶液的pH变化曲线,如图所示,在滴定过程中,关于溶液中离子浓度大小关系的描述不正确的是
的NaOH溶液,溶液的pH变化曲线,如图所示,在滴定过程中,关于溶液中离子浓度大小关系的描述不正确的是
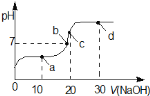
A.a点时:c![]()
![]()
![]()
![]()
![]() (OH-)
(OH-)
B.b点时:c![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
C.c点时:c![]()
![]()
![]()
![]()
![]()
![]()
![]()
D.d点时:c![]()
![]()
![]()
![]()
![]()
![]()
![]()
【答案】A
【解析】
A.![]() 点时醋酸过量,溶液为
点时醋酸过量,溶液为![]() 和
和![]() 的混合物,溶液呈酸性,醋酸根离子的水解程度小于醋酸的电离程度,则
的混合物,溶液呈酸性,醋酸根离子的水解程度小于醋酸的电离程度,则![]() ,故A错误;
,故A错误;
B.根据溶液电荷守恒可知溶液中应存在![]() ,b点是醋酸钠和醋酸的混合溶液,醋酸钠水解后略显碱性,醋酸中和了醋酸钠的碱性,
,b点是醋酸钠和醋酸的混合溶液,醋酸钠水解后略显碱性,醋酸中和了醋酸钠的碱性,![]() 溶液呈中性,则
溶液呈中性,则![]() ,则
,则![]() ,溶液中离子浓度关系为:
,溶液中离子浓度关系为:![]() ,故B正确;
,故B正确;
C.c点时,氢氧化钠与醋酸恰好反应生成醋酸钠溶液,醋酸钠溶液中,根据电荷守恒可得:①![]() ,根据物料守恒可得:②
,根据物料守恒可得:②![]() ,将②带入①可得:
,将②带入①可得:![]() ,故C正确;
,故C正确;
D.d点为NaOH和![]() 的混合物,溶质为
的混合物,溶质为![]() 的醋酸钠和
的醋酸钠和![]() 的氢氧化钠,溶液呈碱性,由于
的氢氧化钠,溶液呈碱性,由于![]() 存在微弱的水解,则有
存在微弱的水解,则有![]() ,故D正确;
,故D正确;
答案选A。

 黄冈创优卷系列答案
黄冈创优卷系列答案【题目】NaOH和盐酸都是中学化学常见的试剂
(一)某同学用0.200 0 mol·L-1标准盐酸滴定待测烧碱溶液浓度
(1)将5.0g烧碱样品( 杂质不与酸反应)配成250 mL待测液,取10.00 mL待测液,用________式滴定管量取,下图是某次滴定时的滴定管中的液面,其读数为________ mL。

(2)由下表数据, NaOH的百分含量是________。
滴定次数 | 待测NaOH溶液体积(mL) | 标准盐酸体积 | |
滴定前的刻度(mL) | 滴定后的刻度(mL) | ||
第一次 | 10.00 | 0.40 | 20.50 |
第二次 | 10.00 | 4.10 | 24.00 |
(3)用标准盐酸滴定某浓度的NaOH溶液,下列操作可能使测定结果偏高的是(_____)
A.用蒸馏水洗锥形瓶后,直接取10.00 mL待测液注入锥形瓶中
B.酸式滴定管在装酸液前未用标准盐酸溶液润洗2—3次
C.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
D.对酸式滴定管,滴定前正确读数,滴定后俯视读数
(二)50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液测定计算中和反应的反应热。回答下列问题:

(4)从实验装置上看,图中缺少的一种玻璃用品是__________。如改用0.0275 mol NaOH固体与该盐酸进行实验,则实验中测得的“中和热”数值将________( 填“偏大”、“偏小”或“无影响”)。
(5)已知盐酸和NaOH稀溶液发生中和反应生成0.1 mol H2O时,放出5.73 kJ的热量,则表示该反应中和热的热化学方程式为:_______________。
(三)常温时,向盛有0.1 mol·L-1Mg2+溶液的试管中滴加适量的NaOH溶液,到pH为11.0时(已知Ksp Mg(OH)2=5.61×1012)
(6)此时上层清液中c(Mg2+)=________ mol·L-1
【题目】硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
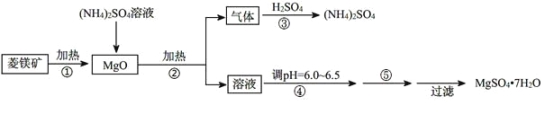
(1)步骤②中发生反应的离子方程式为____________________________________。
(2)步骤④中调节pH=6.0~6.5的目的是___________________________________。
(3)步骤⑤的操作为______________________________
(4)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为_____[25℃时,Ksp[Mg(OH)2] =5.6×10-12]。