题目内容
【题目】(I)![]() 和
和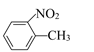 的一些物理性质如下表:
的一些物理性质如下表:
物质 | 熔点 | 沸点 | 密度 | 水溶性 |
| -10℃ | 212℃ | 1.1622g/mL | 不溶于水 |
| 54℃ | 238℃ | 1.1581g/mL | 不溶于水 |
①分离这两种物质混合物可采用的方法是__。(填序号)
A.过滤 B.分液 C.蒸发 D.分馏
②实验需要用到的主要玻璃仪器是___。
(II)酯是重要的有机合成中间体,广泛应用于溶剂、增塑剂、香料、粘合剂及印刷、纺织等工业。乙酸乙酯的实验室和工业制法常采用如下反应:CH3COOH+C2H5OH![]() CH3COOC2H5+H2O
CH3COOC2H5+H2O
请根据要求回答下列问题:
(1)欲提高乙酸的转化率,可采取的措施有___、___等。
(2)若用如图所示装置来制备少量的乙酸乙酯,产率往往偏低,其原因可能为___、___。
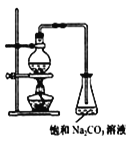
(3)此反应以浓硫酸为催化剂,可能会造成___、__问题。
(4)目前对该反应的催化剂进行了新的探索,初步表明质子酸离子液体可用作反应的催化剂,且能重复使用。实验数据如下表所示(乙酸和乙醇以等物质的量混合)
同一反应时间 | 同一反应温度 | ||||
反应温度/℃ | 转化率(%) | 选择性(%) | 反应时间/h | 转化率(%) | 选择性(%) |
40 | 77.8 | 100 | 2 | 80.2 | 100 |
60 | 92.3 | 100 | 3 | 87.8 | 100 |
80 | 92.6 | 100 | 4 | 92.3 | 100 |
120 | 94.5 | 98.7 | 6 | 93.0 | 100 |
选择性100%表示反应生成的产物是乙酸乙酯和水 | |||||
根据表中数据,下列___(填字母)为该反应的最佳条件。
A.120℃,4h B.80℃,2h
C.60℃,4h D.40℃,3h
【答案】D 冷凝管、蒸馏烧瓶、温度计、牛角管、锥形瓶、酒精灯 增大乙醇的浓度 移去生成物 原料来不及反应就被蒸出 温度过高,发生了副反应或冷凝效果不好,部分产物挥发了 产生大量的酸性废液(或造成环境污染) 部分原料炭化或催化剂重复使用困难或催化效果不理想 C
【解析】
(I)①两种物质常温下为液体,结构相似,则相互溶解,根据表中数据,其沸点不同,可用蒸馏的方法分离;
②蒸馏时,用到的玻璃仪器由由下到上、由左到右的顺序依次为酒精灯、蒸馏烧瓶、温度计、导管、冷凝管、牛角管、锥形瓶;
II(1)乙醇、乙酸均为反应物,提高乙酸的转化率,可增大乙醇的用量,或及时分离出乙酸乙酯等方法;
(2)乙醇易挥发,在加热的条件下还没反应即挥发,或反应温度高副反应较多导致制备少量的乙酸乙酯,产率往往偏低;
(3)以浓硫酸为催化剂,会产生二氧化硫污染环境、高温时,原材料碳化等;
(4)根据表中数据,温度越高耗能越多,转化率提高不明显。
(I)①两种物质常温下为液体,结构相似,则相互溶解,根据表中数据,其沸点不同,可用蒸馏的方法分离,答案为D;
②蒸馏时,用到的玻璃仪器由由下到上、由左到右的顺序依次为酒精灯、蒸馏烧瓶、温度计、导管、冷凝管、牛角管、锥形瓶;
II(1)乙醇、乙酸均为反应物,提高乙酸的转化率,可增大乙醇的用量,或及时分离出乙酸乙酯等方法;
(2)乙醇易挥发,在加热的条件下还没反应即挥发,或反应温度高副反应较多导致制备少量的乙酸乙酯,产率往往偏低;
(3)以浓硫酸为催化剂,会产生二氧化硫污染环境、高温时,原材料碳化等;
(4)根据表中数据,温度越高耗能越多,转化率提高不明显,则选择60℃,4小时,答案为C。