题目内容
【题目】高纯![]() 是广泛用于电子行业的强磁性材料.
是广泛用于电子行业的强磁性材料.![]() 为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于
为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,温度高于![]() 开始分解。
开始分解。
Ⅰ![]() 实验室以
实验室以![]() 为原料制备
为原料制备![]()
![]() 制备
制备![]() 溶液:
溶液:
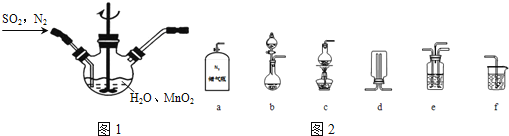
![]() 主要反应装置如图1,缓缓通入经
主要反应装置如图1,缓缓通入经![]() 稀释的
稀释的![]() 气体,发生反应
气体,发生反应![]() ,下列措施中,目的是加快化学反应速率的是______
,下列措施中,目的是加快化学反应速率的是______![]() 填标号
填标号![]() 。
。
A.![]() 加入前先研磨
加入前先研磨![]() 搅拌
搅拌![]() 提高混合气中
提高混合气中![]() 比例
比例
![]() 已知实验室制取
已知实验室制取![]() 的原理是
的原理是![]() 浓
浓![]()
![]()
![]() 选择如图2所示部分装置与图装1置相连制备
选择如图2所示部分装置与图装1置相连制备![]() 溶液,应选择的装置有______
溶液,应选择的装置有______![]() 填标号
填标号![]() .
.
![]() 若用空气代替
若用空气代替![]() 进行实验,缺点是______
进行实验,缺点是______![]() 酸性环境下
酸性环境下![]() 不易被氧化
不易被氧化![]()
![]() 制备
制备![]() 固体:
固体:
实验步骤:![]() 向
向![]() 溶液中边搅拌边加入饱和
溶液中边搅拌边加入饱和![]() 溶液生成
溶液生成![]() 沉淀,反应结束后过滤;
沉淀,反应结束后过滤;![]() ;
;![]() 在
在![]() 下烘干得到纯净干燥的
下烘干得到纯净干燥的![]() 固体。
固体。
步骤![]() 需要用到的试剂有______。
需要用到的试剂有______。
Ⅱ![]() 设计实验方案
设计实验方案
![]() 利用沉淀转化的方法证明
利用沉淀转化的方法证明![]() :______
:______![]() 已知
已知![]() 为难溶于水的浅绿色固体
为难溶于水的浅绿色固体![]()
![]() 证明
证明![]() 的第二步电离不完全:______
的第二步电离不完全:______![]() 查阅资料表明
查阅资料表明![]()
【答案】AB abef 空气中的![]() 能氧化
能氧化![]() ,使
,使![]() 利用率下降 乙醇 向少量
利用率下降 乙醇 向少量![]() 溶液中滴加几滴
溶液中滴加几滴![]() 溶液,生成浅绿色沉淀,再滴加足量
溶液,生成浅绿色沉淀,再滴加足量![]() 溶液,沉淀变成白色 用pH计测量
溶液,沉淀变成白色 用pH计测量![]() 溶液的pH大于7
溶液的pH大于7
【解析】
Ⅰ![]() (1)①根据影响反应速率的因素分析;
(1)①根据影响反应速率的因素分析;
②反应不需要加热制备二氧化硫,b装置制备二氧化硫,氮气与二氧化硫通过e装置混合,在图1装置中反应生成![]() ,利用f进行尾气处理;
,利用f进行尾气处理;
③氧气能与亚硫酸反应生成硫酸;
(2)步骤②为洗涤![]() 沉淀,根据
沉淀,根据![]() 为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化回答;
为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化回答;
Ⅱ![]() (3)根据沉淀转化涉及实验方案;
(3)根据沉淀转化涉及实验方案;
(4)若![]() 的第二步电离不完全,则
的第二步电离不完全,则![]() 能水解。
能水解。
(1)①![]() 研磨、反应时搅拌均可以增大接触面积,加快反应速率,提高混合其中
研磨、反应时搅拌均可以增大接触面积,加快反应速率,提高混合其中![]() 比例,二氧化硫的浓度减小,反应速率减小,故选AB;
比例,二氧化硫的浓度减小,反应速率减小,故选AB;
②反应不需要加热制备二氧化硫,b装置制备二氧化硫,氮气与二氧化硫通过e装置混合,在图1装置中反应生成![]() ,利用f进行尾气处理,防止尾气中二氧化硫污染空气,选abef;
,利用f进行尾气处理,防止尾气中二氧化硫污染空气,选abef;
③制备原理为:![]() ,若用空气代替
,若用空气代替![]() 进行实验,氧气能与亚硫酸反应生成硫酸,二氧化硫利用率降低;
进行实验,氧气能与亚硫酸反应生成硫酸,二氧化硫利用率降低;
(2)步骤②为洗涤![]() ,
,![]() 为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,应用乙醇洗涤,可以防止被氧化;
为白色粉末,不溶于水和乙醇,在潮湿环境下易被氧化,应用乙醇洗涤,可以防止被氧化;
(3)先向少量![]() 溶液中滴加几滴
溶液中滴加几滴![]() 溶液,生成浅绿色沉淀,再滴加足量
溶液,生成浅绿色沉淀,再滴加足量![]() 溶液,沉淀变成白色,可证明
溶液,沉淀变成白色,可证明![]() ;
;
(4) 若![]() 的第二步电离不完全,则
的第二步电离不完全,则![]() 能水解,用pH计测量
能水解,用pH计测量![]() 溶液的pH大于7,可证明
溶液的pH大于7,可证明![]() 的第二步电离不完全。
的第二步电离不完全。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案【题目】I. 现有一组物质的熔点(℃)数据,据此回答下列问题:
HF:-83 | HCl:-115 | HBr:-89 | HI:-51 |
(1)HF熔点反常是由于______________。这组物质中共价键的键能最大的是_____。
II.按要求回答下列问题。
(2)CS2气化时克服的粒子间作用是__________,1mol CS2中含有___mol σ键,含有___mol π键。
(3)HCHO分子中C原子轨道的杂化类型为______。