题目内容
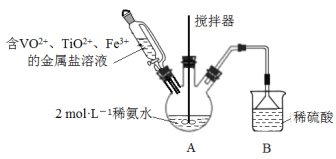
【题目】(1)氯化铁水解的离子方程式为_________________________________,加热氯化铁溶液,蒸干并灼烧得到_______(填化学式)。
(2)25℃时,NH4Cl溶液显_________性,原因是(用离子方程式表示)__________,若加入少量的氨水,使溶液中c(NH4+)=c(Cl﹣),则溶液的pH___7(填“>”、“<”或“=”)
【答案】Fe3+ + 3H2O![]() Fe(OH)3 + 3H+ Fe2O3 酸 NH4+ + H2O
Fe(OH)3 + 3H+ Fe2O3 酸 NH4+ + H2O![]() NH3·H2O + H+ =
NH3·H2O + H+ =
【解析】
(1)氯化铁属于强酸弱碱盐,铁离子水解显酸性,据水解规律写出离子方程式;氯化铁水解产生的盐酸受热易挥发,因此加热氯化铁溶液,蒸干并灼烧得到氧化铁固体;
(2)氯化铵溶液中铵根离子水解使溶液显酸性;根据电荷守恒判断出c(H+)与 c(OH-)关系,进而判定pH与7之间的关系。
(1)氯化铁属于强酸弱碱盐,铁离子水解显酸性,水解的离子方程式为Fe3+ +3H2O![]() Fe(OH)3 + 3H+,水解后产生的盐酸具有挥发性,因此加热氯化铁溶液,蒸干的过程中,盐酸的浓度不断减小,平衡右移,生成了氢氧化铁固体,该固体再被灼烧,氢氧化铁分解为氧化铁和水,最终可以得到Fe2O3固体;
Fe(OH)3 + 3H+,水解后产生的盐酸具有挥发性,因此加热氯化铁溶液,蒸干的过程中,盐酸的浓度不断减小,平衡右移,生成了氢氧化铁固体,该固体再被灼烧,氢氧化铁分解为氧化铁和水,最终可以得到Fe2O3固体;
综上所述,本题答案是:Fe3++3H2O![]() Fe(OH)3 +3H+ ,Fe2O3。
Fe(OH)3 +3H+ ,Fe2O3。
(2)氯化铵溶液中因为铵根离子的水解,使溶液显酸性,铵根水解的离子方程式为NH4+ + H2O![]() NH3·H2O + H+ ,加入氨水导致c(NH4+)=c(Cl﹣),据电荷守恒c(NH4+)+c(H+)= c(Cl﹣)+c(OH-),c(H+)= c(OH-),则有氢离子浓度与氢氧根离子浓度相等,都是10-7mol/L, pH=7;
NH3·H2O + H+ ,加入氨水导致c(NH4+)=c(Cl﹣),据电荷守恒c(NH4+)+c(H+)= c(Cl﹣)+c(OH-),c(H+)= c(OH-),则有氢离子浓度与氢氧根离子浓度相等,都是10-7mol/L, pH=7;
因此,本题正确答案是: 酸,NH4+ + H2O![]() NH3·H2O + H+, =。
NH3·H2O + H+, =。

 综合自测系列答案
综合自测系列答案【题目】根据下列实验操作和现象所得出的结论正确的是
选项 | 实验操作和现象 | 结论 |
A | 向苯酚浊液中滴加Na2CO3溶液,浊液变清 | 苯酚的酸性强于H2CO3的酸性 |
B | 将 KI 溶液滴入 FeCl3 溶液中,加入 CCl4,振荡、静置,下层溶液显紫色 | 还原性:Fe2+>I |
C | 向含酚酞的 Na2CO3 溶液中加入 BaCl2 溶液,红色褪去 | Na2CO3 溶液中存在水解平衡 |
D | 某无色溶液中滴加稀NaOH溶液,将湿润的红色石蕊试纸置于试管口,试纸不变蓝 | 原溶液中一定无 NH4+ |
A. AB. BC. CD. D
【题目】下表是周期表中的一部分,根据①--⑩在周期表中的位置,用元素符号或化学式回答下列问题:
族周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
1 | ① | |||||||
2 | ④ | ⑦ | ⑧ | ⑩ | ||||
3 | ② | ③ | ⑤ | ⑥ | ⑨ |
(1)表中元素,化学性质最不活泼的是______,还原性最强的单质是______,可用于制半导体材料的元素是______;
(2)在②、③、④、⑤、⑥、⑦、⑧、⑨中,原子半径最大的是______;
(3)比较⑥、⑦、⑨的氢化物的稳定性最弱的是______;
(4)铍![]() 位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加______(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式__________。
位于元素周期表中第二周期第ⅡA族。相同条件下,单质铍与酸反应比单质锂与酸反应更加______(填“剧烈”或“缓慢”),写出铍与盐酸反应的化学方程式__________。
【题目】无水氯化铝在生产、生活中应用广泛。
(1)氯化铝水溶液呈_____性,原因是(用离子方程式表示)________;把AlCl3溶液蒸干,灼烧,最后得到的主要固体产物是_______。
(2)工业上用铝土矿(主要成分为Al2O3,含有Fe2O3、SiO2等杂质)制取无水氯化铝的一种工艺流程示意如下:
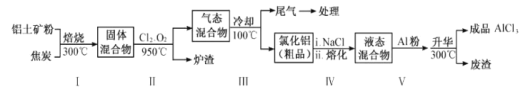
已知:
物质 | SiCl4 | AlCl3 | FeCl3 | FeCl2 |
沸点/℃ | 57.6 | 180(升华) | 300(升华) | 1023 |
①步骤Ⅰ中焙烧使固体水分挥发、气孔数目增多,其作用是___________(只要求写出一种)。
②步骤Ⅱ中若不通入氯气和氧气,则反应生成相对原子质量比硅大的单质是_____。
③ 已知:
Al2O3(s)+3C(s)=2Al(s)+3CO(g) ΔH1=+1344.1kJ ·mol-1
2AlCl3(g)=2Al(s)+3Cl2(g) ΔH2=+1169.2kJ ·mol-1
由Al2O3、C和Cl2反应生成AlCl3的热化学方程式为______________。
④步骤Ⅲ经冷却至室温后,气体用足量的NaOH冷溶液吸收,生成的盐主要有3种,其化学式分别为_______、 _______ 、 _________。
⑤结合流程及相关数据分析,步骤Ⅴ中加入铝粉的目的是___________________。