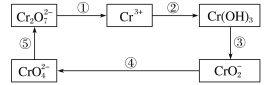
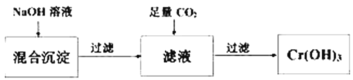
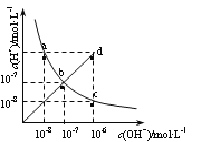
题目内容
【题目】下列说法正确的是![]()
A.向50mL![]() 的盐酸中加入烧碱后,水的
的盐酸中加入烧碱后,水的![]() 不变
不变
B.![]() 和
和![]() 混合液中,二者对对方的平衡都起了抑制作用
混合液中,二者对对方的平衡都起了抑制作用
C.室温时某溶液的![]() ,则该物质一定是酸或强酸弱碱盐
,则该物质一定是酸或强酸弱碱盐
D.常温下![]()
![]() 的HA溶液中
的HA溶液中 ,则
,则![]()
![]() 溶液中
溶液中![]()
![]()
【答案】B
【解析】
A.![]() 只受温度的影响,盐酸中加入烧碱发生酸碱中和反应,放出热量,使体系温度升高,Kw值增大,故A错误;
只受温度的影响,盐酸中加入烧碱发生酸碱中和反应,放出热量,使体系温度升高,Kw值增大,故A错误;
B.铵根离子水解方程式:![]() ,加入一水合氨,一水合氨浓度增大,平衡向逆向移动,抑制铵根离子的水解;一水合氨的电离方程式:
,加入一水合氨,一水合氨浓度增大,平衡向逆向移动,抑制铵根离子的水解;一水合氨的电离方程式:![]() ,加入氯化铵溶液,铵根离子浓度增大,平衡向逆向移动,抑制了一水合氨的电离,故B正确;
,加入氯化铵溶液,铵根离子浓度增大,平衡向逆向移动,抑制了一水合氨的电离,故B正确;
C.室温时某溶液的![]() ,可能为酸或强酸弱碱盐或酸式盐,如
,可能为酸或强酸弱碱盐或酸式盐,如![]() ,故C错误;
,故C错误;
D.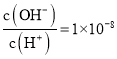 ,
,![]() ,所以
,所以![]() ,该酸为弱酸,加水稀释时弱酸的电离程度增大,所以
,该酸为弱酸,加水稀释时弱酸的电离程度增大,所以![]() 溶液中
溶液中![]() ,故D错误;
,故D错误;
故答案为B。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案【题目】700 ℃时,向容积为2 L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g) CO2(g)+H2(g),反应过程中测定的部分数据见下表(表中t2>t1):
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 1.20 | 0.60 |
t1 | 0.20 | |
t2 | 0.80 |
依据题意回答下列问题:
(1)反应在t1 min内的平均速率为v(H2)=________ mol·L-1·min-1。
(2)保持其他条件不变,起始时向容器中充入0.60 mol CO和1.20 mol H2O,到达平衡时,n(CO2)=________mol。
(3)温度升至800 ℃,上述反应的平衡常数为0.64,则正反应为________反应(填“放热”或“吸热”)。
(4)700 ℃时,向容积为2 L的密闭容器中充入CO(g)、H2O(g)、CO2(g)、H2(g)的物质的量分别为1.20 mol、2.00 mol、1.20 mol、1.20 mol,则此时该反应v(正)________v(逆)(填“>”“<”或“=”)。
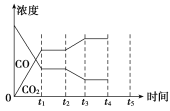
(5)该反应在t1时刻达到平衡,在t2时刻因改变某个条件,CO和CO2浓度发生变化的情况如图所示。图中t2时刻发生改变的条件可能是________或________。
(6)若该容器容积不变,能说明反应达到平衡的是________。
①c(CO)与c(H2)的比值保持不变
②v(CO2)正=v(H2O)逆
③体系的压强不再发生变化
④混合气体的密度不变
⑤体系的温度不再发生变化
⑥气体的平均相对分子质量不变