题目内容
下列除杂方案正确的是(括号内为除杂剂)( )
| A、NaOH溶液中混有Ba(OH)2(K2SO4) |
| B、NaCl溶液中混有Na2CO3(盐酸) |
| C、CO中混有CO2(炽热的炭) |
| D、CO2中混有HCl气体(NaOH溶液) |
考点:物质的分离、提纯的基本方法选择与应用,物质的分离、提纯和除杂
专题:实验评价题
分析:A.氢氧化钡与硫酸钾反应生成硫酸钡和KOH;
B.碳酸钠与盐酸反应生成NaCl、水和二氧化碳;
C.加热下CO可被氧化;
D.二者均与NaOH溶液反应.
B.碳酸钠与盐酸反应生成NaCl、水和二氧化碳;
C.加热下CO可被氧化;
D.二者均与NaOH溶液反应.
解答:
解:A.氢氧化钡与硫酸钾反应生成硫酸钡和KOH,引入新杂质,应选硫酸钠,故A错误;
B.碳酸钠与盐酸反应生成NaCl、水和二氧化碳,则加盐酸可除杂,故B正确;
C.加热下CO可被氧化,应利用NaOH溶液、洗气来除杂,故C错误;
D.二者均与NaOH溶液反应,应利用饱和碳酸氢钠溶液来除杂,故D错误;
故选B.
B.碳酸钠与盐酸反应生成NaCl、水和二氧化碳,则加盐酸可除杂,故B正确;
C.加热下CO可被氧化,应利用NaOH溶液、洗气来除杂,故C错误;
D.二者均与NaOH溶液反应,应利用饱和碳酸氢钠溶液来除杂,故D错误;
故选B.
点评:本题考查物质分离、提纯方法及选择,为高频考点,把握物质的性质及性质差异为解答的关键,注意发生的反应和除杂的原则,题目难度不大.

练习册系列答案
相关题目
下列化学变化中,必须加入氧化剂才能实现的是( )
| A、SO2→H2SO3 |
| B、Cl2→NaClO |
| C、Fe→FeCl2 |
| D、HNO3→O2 |
短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2mol ECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀.下列判断错误的是( )
| A、E是一种非金属元素 |
| B、在ECln中E与Cl之间形成共价键 |
| C、E的一种常见氧化物为EO |
| D、E位于元素周期表的ⅥA族 |
下列物质的水溶液,加热蒸干得到原物质的是( )
①NaAlO2 ②FeCl3 ③CuSO4 ④FeSO4 ⑤Na2S ⑥Ca(HCO3)2 ⑦NaClO ⑧NH4I ⑨Na2SO3 ⑩CaCl2.
①NaAlO2 ②FeCl3 ③CuSO4 ④FeSO4 ⑤Na2S ⑥Ca(HCO3)2 ⑦NaClO ⑧NH4I ⑨Na2SO3 ⑩CaCl2.
| A、①③⑤⑥⑧⑩ |
| B、②③④⑤⑨⑩ |
| C、①③⑤⑩ |
| D、③⑤⑦⑩ |
下列关于Fe(OH)3胶体的说法中不正确的是( )
| A、Fe(OH)3胶体与硅酸溶液混合将产生凝聚现象 |
| B、Fe(OH)3胶体粒子在电场影响下将向阳极移动 |
| C、液溶胶中Fe(OH)3胶体粒子不停地做布朗运动 |
| D、光线通过Fe(OH)3胶体时会发生丁达尔现象 |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,48g O3含有的氧原子数目为3NA |
| B、2.4g金属镁变为离子时失去电子的数目为0.1NA |
| C、含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| D、物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数目为NA |
下列关于化石燃料及其加工说法正确的是( )
| A、天然气和沼气的主要成分都是甲烷,二者都是不可再生资源 |
| B、石油分馏和煤千馏都是物理变化,前者可得到汽油、煤油等,后者主要得到焦炭、煤焦油、粗氨水和焦炉气 |
| C、石油裂化主要是为了提高轻质油的产量,尤其是汽油的产量 |
| D、煤的液化指的是把煤加热到熔点以上使其变成液体 |
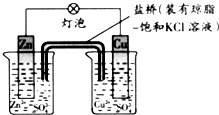 铜锌原电池工作时,下列叙述正确的是( )
铜锌原电池工作时,下列叙述正确的是( )| A、正极反应为:Zn-2e-=Zn2+ |
| B、在外电路中,电子从铜片流向锌片 |
| C、电池反应为:Zn+Cu2+=Zn2++Cu |
| D、盐桥中的K+移向ZnSO4溶液 |
 如图为一个电化学过程的示意图.请回答下列问题:
如图为一个电化学过程的示意图.请回答下列问题: