题目内容
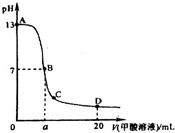 甲酸为一元弱酸,在15mL 0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线.下面有关微粒浓度的大小关系正确的是( )
甲酸为一元弱酸,在15mL 0.1mol/L KOH溶液中逐滴加入0.2mol/L甲酸溶液,溶液的pH变化和所加入的甲酸的体积关系描绘成如图所示曲线.下面有关微粒浓度的大小关系正确的是( )| A、在A、B间的任意一点上都存在:c(K+)>c(HCOO-)>c(OH-)>c(H+) |
| B、在B点:c(K+)=c(HCOO-)>c(OH-)=c(H+),且a=7.5 |
| C、在C点:c(HCOO-)>c(K+)>(H+)>c(OH-) |
| D、在D点:c(HCOO-)+c(HCOOH)=2c(K+) |
考点:离子浓度大小的比较,酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:A.开始时c(OH-)>c(HCOO-),所以A、B之间不一定满足c(HCOO-)>c(OH-);
B.当恰好中和时消耗0.2mol/L甲酸溶液7.5mL,溶液显示碱性,欲显中性,甲酸应该稍过量,则有a>7.5;
C.在C点甲酸过量,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒可知c(HCOO-)>c(K+);
D.点甲酸过量,所加入甲酸的物质的量大于KOH的物质的量的2倍,根据物料守恒进行判断.
B.当恰好中和时消耗0.2mol/L甲酸溶液7.5mL,溶液显示碱性,欲显中性,甲酸应该稍过量,则有a>7.5;
C.在C点甲酸过量,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒可知c(HCOO-)>c(K+);
D.点甲酸过量,所加入甲酸的物质的量大于KOH的物质的量的2倍,根据物料守恒进行判断.
解答:
解:A.在A、B间任意一点,因为开始时c(OH-)>c(HCOO-),即有可能存在:c(K+)>c(OH-)>c(HCOO-)>c(H+),故A错误;
B.当恰好中和时消耗0.2mol/L甲酸溶液7.5mL,反应生成甲酸钠溶液,溶液显示碱性,若溶液为中性,则c(OH-)=c(H+),根据电荷守恒c(K+)=c(HCOO-),由于溶液中存在部分甲酸,则应该满足a>7.5,故B错误;
C.C点甲酸过量,溶液呈酸性,c(H+)>c(OH-),由电荷守恒可得c(HCOO-)>c(K+),所以溶液中离子浓度大小为:c(HCOO-)>c(K+)>c(H+)>c(OH-),故C正确;
D.D点甲酸过量,所加入甲酸的物质的量为:0.02L×0.2mol/L═0.004mol,KOH的物质的量为:0.015L×0.1mol/L=0.0015mol,根据物料守恒,则反应后溶液中一定满足:c(HCOO-)+c(HCOOH)>2c(K+),故D错误;
故选C.
B.当恰好中和时消耗0.2mol/L甲酸溶液7.5mL,反应生成甲酸钠溶液,溶液显示碱性,若溶液为中性,则c(OH-)=c(H+),根据电荷守恒c(K+)=c(HCOO-),由于溶液中存在部分甲酸,则应该满足a>7.5,故B错误;
C.C点甲酸过量,溶液呈酸性,c(H+)>c(OH-),由电荷守恒可得c(HCOO-)>c(K+),所以溶液中离子浓度大小为:c(HCOO-)>c(K+)>c(H+)>c(OH-),故C正确;
D.D点甲酸过量,所加入甲酸的物质的量为:0.02L×0.2mol/L═0.004mol,KOH的物质的量为:0.015L×0.1mol/L=0.0015mol,根据物料守恒,则反应后溶液中一定满足:c(HCOO-)+c(HCOOH)>2c(K+),故D错误;
故选C.
点评:本题考查酸碱混合溶液PH的判断与计算,这是一道以中和滴定为背景,以图象呈现为方式的离子浓度大小比较题,题目难度中等,注意从电解质的强弱以及酸碱混合反应的角度分析,注意分析曲线的变化特点.

练习册系列答案
 作业辅导系列答案
作业辅导系列答案
相关题目
短周期元素E的氯化物ECln的熔点为-78℃,沸点为59℃;若0.2mol ECln与足量的AgNO3溶液完全反应后可以得到57.4g的AgCl沉淀.下列判断错误的是( )
| A、E是一种非金属元素 |
| B、在ECln中E与Cl之间形成共价键 |
| C、E的一种常见氧化物为EO |
| D、E位于元素周期表的ⅥA族 |
下列关于Fe(OH)3胶体的说法中不正确的是( )
| A、Fe(OH)3胶体与硅酸溶液混合将产生凝聚现象 |
| B、Fe(OH)3胶体粒子在电场影响下将向阳极移动 |
| C、液溶胶中Fe(OH)3胶体粒子不停地做布朗运动 |
| D、光线通过Fe(OH)3胶体时会发生丁达尔现象 |
设NA表示阿伏加德罗常数,下列叙述中正确的是( )
| A、常温常压下,48g O3含有的氧原子数目为3NA |
| B、2.4g金属镁变为离子时失去电子的数目为0.1NA |
| C、含有NA个氦原子的氦气在标准状况下的体积约为11.2L |
| D、物质的量浓度为0.5mol/L MgCl2溶液,含有Cl-离子数目为NA |
下列电离方程式中正确的是( )
| A、H2SO4=H2++SO42- |
| B、NaHCO3=Na++H++CO32- |
| C、Ca(OH)2=Ca2++2OH- |
| D、CaCl2=Ca+2+2Cl- |
下列关于化石燃料及其加工说法正确的是( )
| A、天然气和沼气的主要成分都是甲烷,二者都是不可再生资源 |
| B、石油分馏和煤千馏都是物理变化,前者可得到汽油、煤油等,后者主要得到焦炭、煤焦油、粗氨水和焦炉气 |
| C、石油裂化主要是为了提高轻质油的产量,尤其是汽油的产量 |
| D、煤的液化指的是把煤加热到熔点以上使其变成液体 |
NA表示阿伏加德罗常数,下列叙述正确的是( )
| A、32g硫在足量的O2中燃烧生成的SO3分子数等于NA |
| B、1mol Cl2与足量的NaOH溶液反应,转移的电子数为2NA |
| C、常温常压下,25g甲醛所含电子数为10NA |
| D、在标准状态下,68g H2O2中含有的6mol共价键 |
下列反应离子方程式表示不正确的是( )
| A、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
| B、Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O |
| C、向明矾[KAl(SO4)2]溶液中逐滴加入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-=2Al(OH)3↓+3BaSO4↓ |
| D、向次氯酸钠溶液中通入少量SO2:ClO-+SO2+H2O=Cl-+SO42-+2H+ |