题目内容
13.常见锌锰干电池因含有汞、酸或碱等,废弃后进入环境将造成严重危害.某化学兴趣小组拟采用如图1处理方法回收废电池中的各种资源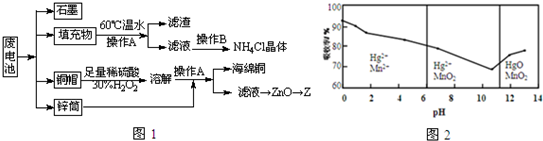
(1)操作A的名称为过滤.
(2)铜帽溶解时加入H2O2的目的是Cu+H2O2+H2SO4=CuSO4+2H2O;(用化学方程式表示).铜帽溶解完全后,可采用加热方法除去溶液中过量的H2O2.
(3)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,其负极的电极反应式为Zn+2OH--2e-=Zn(OH)2.
(4)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.
①当1mol MnO2参加反应时,共有4mol电子发生转移.
②MnO (OH)与浓盐酸在加热条件下也可发生反应,试写出该反应的化学方程式:2MnO(OH)+6HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2MnCl2+Cl2↑+4H2O.
(5)锌锰干电池所含的汞可用KMnO4溶液吸收.在不同pH下,KMnO4溶液对Hg的吸收率及主要产物如图2所示,根据图2可知:
①pH对Hg吸收率的影响规律是随pH升高,汞的吸收率先降低后增加.
②在强酸性环境下Hg的吸收率高的原因可能是KMnO4在酸性条件下氧化性强.
分析 废旧干电池含有铜、石墨、二氧化锰以及填充物等,填充物用60℃充分溶解,过滤,滤液中含有氯化铵,蒸发、浓缩、结晶可得到氯化铵晶体;铜与稀硫酸在过氧化氢作用发生氧化还原反应生成硫酸铜,加入锌可置换出铜,过滤分离,硫酸锌溶液最终可生成氢氧化锌、氧化锌,冶炼可得到锌,
(1)操作A用于分离固体和液体;
(2)酸性条件下,双氧水能将铜氧化生成铜离子;加热条件下,双氧水易分解;
(3)碱性锌锰干电池的电解质为KOH,总反应为Zn+2MnO2+2H2O═2MnOOH+Zn(OH)2,其负极上锌失电子发生氧化反应;
(4)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.其主要反应为2MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.
①根据二氧化锰和转移电子之间的关系式计算;
②MnO(OH)与浓盐酸在加热条件下也可发生反应生成氯化锰、氯气和水;
(5)根据横坐标与其吸收率曲线变化趋势分析;酸性条件下,高锰酸钾具有强氧化性.
解答 解:废旧干电池含有铜、石墨、二氧化锰以及填充物等,填充物用60℃充分溶解,过滤,滤液中含有氯化铵,蒸发、浓缩、结晶可得到氯化铵晶体;铜与稀硫酸在过氧化氢作用发生氧化还原反应生成硫酸铜,加入锌可置换出铜,过滤分离,硫酸锌溶液最终可生成氢氧化锌、氧化锌,冶炼可得到锌,
(1)分离不溶性固体和溶液采用过滤的方法,所以该操作名称是过滤,
故答案为:过滤;
(2)酸性条件下,双氧水能将铜氧化生成铜离子反应的化学方程式为:Cu+H2O2+H2SO4=CuSO4+2H2O;加热条件下,双氧水易分解生成水和氧气,所以除去双氧水的方法是加热,
故答案为:Cu+H2O2+H2SO4=CuSO4+2H2O; 加热;
(3)负极发生氧化反应,由方程式可知Zn被氧化生成Zn(OH)2,则电极方程式为Zn+2OH--2e-=Zn(OH)2,
故答案为:Zn+2OH--2e-=Zn(OH)2;
(4)滤渣的主要成分为含锰混合物,向含锰混合物中加入一定量的稀硫酸、稀草酸,并不断搅拌至无气泡为止.其主要反应为2 MnO(OH)+MnO2+2H2C2O4+3H2SO4═3MnSO4+4CO2↑+6H2O.
①该反应中,氧化剂是MnO(OH)、MnO2,还原剂是草酸,当1mol MnO2参加反应时,转移电子的物质的量=$\frac{1mol}{1}$=4mol,
故答案为:4;
②MnO(OH)与浓盐酸在加热条件下也可发生反应生成氯化锰、氯气和水,反应方程式为:2MnO(OH)+6HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2MnCl2+Cl2↑+4H2O,
故答案为:2MnO(OH)+6HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2MnCl2+Cl2↑+4H2O;
(5)①根据图象知,随着pH的增大,汞的吸收率先先降低后增加,
故答案为:先降低后增加;
②酸性条件下,高锰酸钾具有强氧化性,所以酸性条件下的高锰酸钾氧化性更强,
故答案为:氧化性.
点评 本题考查了物质的分离和提纯、原电池原理,根据原电池正负极上发生的反应、物质的性质及其分离方法来分析解答,能从整体上把握物质分离过程,熟练掌握基础知识,灵活运用知识解答,题目难度中等.

| A. | (NH4)2 SO4 | B. | Al(OH)3 | C. | NaHSO4 | D. | Mg(NO3)2 |
| A. | 少量浓硫酸沾到皮肤上,立即用氢氧化钠溶液冲洗 | |
| B. | 制取并收集氧气结束后,应立即停止加热 | |
| C. | 当出现CO中毒时,应立即将中毒者抬到室外新鲜空气处 | |
| D. | 将含硫酸的废液倒入水槽,用水冲入下水道 |
| 步骤 | 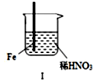 |  | |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe Cu接触后,其表面均产生红棕色气泡 |
| A. | Ⅰ中气体有无色变红棕色的化学方程式为:2NO+O2=2NO2 | |
| B. | 对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 | |
| C. | Ⅱ中的现象说明Fe表面形成致密的氧化层,阻止Fe进一步反应 | |
| D. | 针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
 ;该反应中,氧化产物是Cl2,还原产物是Cl2,氧化产物与还原产物的物质的量之比是5:1.
;该反应中,氧化产物是Cl2,还原产物是Cl2,氧化产物与还原产物的物质的量之比是5:1. | A. | 金属焊接时可用NH4Cl溶液作除锈剂 | |
| B. | 配制FeSO4溶液时,加入一定量Fe粉 | |
| C. | 长期施用铵态氮肥会使土壤酸化 | |
| D. | 向FeCl3溶液中加入CaCO3粉末后有气泡产生 |
 (用电子式表示).
(用电子式表示).