题目内容
按要求填空:
(1)新制的氯水的保存方法: ,用化学方程式说明原因: ;
(2)氯气有毒,常用 溶液吸收实验中多余的Cl2,反应的化学方程式: ;
(3)向饱和的碳酸钠溶液中通入CO2,现象: ,反应的化学方程式: ;
(4)除去NaCl固体中混有的少量CaCO3,所进行的实验操作为: 、 、蒸发、结晶.
(5)除去NaCl中的Na2SO4,依次加入的溶液为(填溶质化学式): 、 、 .
(6)下列物质中①铜、②NaCl溶液、③熔融的KNO3、④NaCl、⑤Ba(OH)2固体、⑥纯H2SO4、⑦NH3⑧CO2、⑨蔗糖(用序号填写),属于电解质的是 ,属于非电解质的是 ,能导电的是 .
(1)新制的氯水的保存方法:
(2)氯气有毒,常用
(3)向饱和的碳酸钠溶液中通入CO2,现象:
(4)除去NaCl固体中混有的少量CaCO3,所进行的实验操作为:
(5)除去NaCl中的Na2SO4,依次加入的溶液为(填溶质化学式):
(6)下列物质中①铜、②NaCl溶液、③熔融的KNO3、④NaCl、⑤Ba(OH)2固体、⑥纯H2SO4、⑦NH3⑧CO2、⑨蔗糖(用序号填写),属于电解质的是
考点:氯气的化学性质,电解质与非电解质,电解质溶液的导电性,钠的重要化合物,物质的分离、提纯和除杂
专题:电离平衡与溶液的pH专题,卤族元素,化学实验基本操作
分析:(1)新制氯水中的次氯酸不稳定,易分解,次氯酸分解得到盐酸和氧气;
(2)氯气有毒,可以和强碱反应,据此用氢氧化钠来进行尾气处理;
(3)碳酸钠的溶解度大于碳酸氢钠的溶解度,碳酸盐和二氧化碳、水反应可以得到碳酸氢盐;
(4)碳酸钙不溶于水,NaCl溶于水;
(5)Na2SO4与氯化钡反应生成NaCl和硫酸钡沉淀,再利用碳酸钠除去氯化钡,最后利用盐酸除杂;
(6)在水溶液中或熔化状态下导电的化合物,为电解质;在水溶液中和熔化状态下导电的化合物,为非电解质,注意电解质必须本身电离;具有自由移动的离子或电子,可导电,以此来解答.
(2)氯气有毒,可以和强碱反应,据此用氢氧化钠来进行尾气处理;
(3)碳酸钠的溶解度大于碳酸氢钠的溶解度,碳酸盐和二氧化碳、水反应可以得到碳酸氢盐;
(4)碳酸钙不溶于水,NaCl溶于水;
(5)Na2SO4与氯化钡反应生成NaCl和硫酸钡沉淀,再利用碳酸钠除去氯化钡,最后利用盐酸除杂;
(6)在水溶液中或熔化状态下导电的化合物,为电解质;在水溶液中和熔化状态下导电的化合物,为非电解质,注意电解质必须本身电离;具有自由移动的离子或电子,可导电,以此来解答.
解答:
解:(1)新制氯水中的次氯酸不稳定,易分解,次氯酸分解得到盐酸和氧气,反应为2HClO
2HCl+O2↑,所以新制的氯水保犯法:棕色试剂瓶遮光保存,
故答案为:棕色试剂瓶遮光保存;2HClO
2HCl+O2↑;
(2)氯气有毒,可以和强碱反应,常用氢氧化钠来进行尾气处理,反应为Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:NaOH;Cl2+2NaOH=NaCl+NaClO+H2O;
(3)向碳酸钠溶液中通入二氧化碳可以发生反应得到碳酸氢钠溶液,由于碳酸钠的溶解度大于碳酸氢钠的溶解度,所以会出现白色浑浊,即Na2CO3+CO2+H2O=2NaHCO3↓,故答案为:出现白色浑浊;Na2CO3+CO2+H2O=2NaHCO3↓;
(4)碳酸钙不溶于水,NaCl溶于水,则所进行的实验操作为:溶解、过滤、蒸发、结晶,故答案为:溶解;过滤;
(5)Na2SO4与氯化钡反应生成NaCl和硫酸钡沉淀,再利用碳酸钠除去氯化钡,最后利用盐酸除杂,则除杂依次加入的溶液为BaCl2、Na2CO3、HCl,
故答案为:BaCl2;Na2CO3;HCl;
(6)①铜为单质,可导电,既不是电解质也不是非电解质;
②NaCl溶液为混合物,可导电,既不是电解质也不是非电解质;
③熔融的KNO3可导电,为电解质;
④NaCl不能导电,是在水溶液中或熔化状态下导电的化合物,为电解质;
⑤Ba(OH)2固体不能导电,是在水溶液中或熔化状态下导电的化合物,为电解质;
⑥纯H2SO4不能导电,是在水溶液中导电的化合物,为电解质;
⑦NH3不能导电,本身不能电离,为非电解质;
⑧CO2不能导电,本身不能电离,为非电解质;
⑨蔗糖不能导电,本身不能电离,为非电解质,则属于电解质的是③④⑤⑥,属于非电解质的是⑦⑧⑨,能导电的是①②③,
故答案为:③④⑤⑥;⑦⑧⑨;①②③.
| ||
故答案为:棕色试剂瓶遮光保存;2HClO
| ||
(2)氯气有毒,可以和强碱反应,常用氢氧化钠来进行尾气处理,反应为Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:NaOH;Cl2+2NaOH=NaCl+NaClO+H2O;
(3)向碳酸钠溶液中通入二氧化碳可以发生反应得到碳酸氢钠溶液,由于碳酸钠的溶解度大于碳酸氢钠的溶解度,所以会出现白色浑浊,即Na2CO3+CO2+H2O=2NaHCO3↓,故答案为:出现白色浑浊;Na2CO3+CO2+H2O=2NaHCO3↓;
(4)碳酸钙不溶于水,NaCl溶于水,则所进行的实验操作为:溶解、过滤、蒸发、结晶,故答案为:溶解;过滤;
(5)Na2SO4与氯化钡反应生成NaCl和硫酸钡沉淀,再利用碳酸钠除去氯化钡,最后利用盐酸除杂,则除杂依次加入的溶液为BaCl2、Na2CO3、HCl,
故答案为:BaCl2;Na2CO3;HCl;
(6)①铜为单质,可导电,既不是电解质也不是非电解质;
②NaCl溶液为混合物,可导电,既不是电解质也不是非电解质;
③熔融的KNO3可导电,为电解质;
④NaCl不能导电,是在水溶液中或熔化状态下导电的化合物,为电解质;
⑤Ba(OH)2固体不能导电,是在水溶液中或熔化状态下导电的化合物,为电解质;
⑥纯H2SO4不能导电,是在水溶液中导电的化合物,为电解质;
⑦NH3不能导电,本身不能电离,为非电解质;
⑧CO2不能导电,本身不能电离,为非电解质;
⑨蔗糖不能导电,本身不能电离,为非电解质,则属于电解质的是③④⑤⑥,属于非电解质的是⑦⑧⑨,能导电的是①②③,
故答案为:③④⑤⑥;⑦⑧⑨;①②③.
点评:本题考查较综合,涉及氯气的化学性质、碳酸钠和碳酸钠的性质以及次氯酸的不稳定性、混合物分离提纯、电解质与非电解质等知识,注重基础知识的考查,题目难度不大.

练习册系列答案
相关题目
短周期元素R、T、X、Y、Z在元素周期表的相对位置如下表所示,它们的最外层电子数之和为29.则下列判断正确的是( )
| R | T | |
| X | Y | Z |
| A、R位于元素周期表中第二周期第ⅣA族 |
| B、五种元素中原子半径最大的是X |
| C、气态氢化物稳定性:Y>T |
| D、Z元素的最高价氧化物对应的水化物的化学式为HZO4 |
用NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,NA个己烷分子所占的体积约为22.4L |
| B、常温常压下,4g氦气含NA个原子 |
| C、1mol NaHCO3晶体中含有NA个CO32- |
| D、1mol Na2O2与足量的CO2气体充分反应后,转移的电子总数为2NA个 |
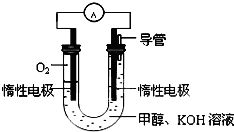 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景.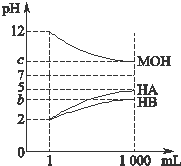 为研究HA、HB溶液和MOH的酸碱性的相对强弱,某化学学习小组设计了以下实验:室温下,将pH=2的两种酸溶液HA、HB和pH=12的碱溶液MOH各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图所示,根据所给数据,请回答下列问题:
为研究HA、HB溶液和MOH的酸碱性的相对强弱,某化学学习小组设计了以下实验:室温下,将pH=2的两种酸溶液HA、HB和pH=12的碱溶液MOH各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图所示,根据所给数据,请回答下列问题: