题目内容
元素X、Y的单质是生活中常见的金属,A、B、C、D、E是中学常见的5种化合物,其中A、B是氧化物,试剂1为氢氧化钠,试剂2是稀硫酸.相关物质间的关系如图.
(1)写出下列物质的化学式
A、 C、 Y、 D、 .
(2)检验物质D的溶液中金属离子的方法是 .
(3)将物质D溶于水,其溶液呈酸性,原因是(用离子方程式表示) .

(1)写出下列物质的化学式
A、
(2)检验物质D的溶液中金属离子的方法是
(3)将物质D溶于水,其溶液呈酸性,原因是(用离子方程式表示)
考点:无机物的推断
专题:推断题
分析:元素X、Y的单质是生活中常见的金属,分别为Al、Fe中的一种,且X与氧化物A反应得到Y与氧化物B,则X为Al,Y为Fe,B为氧化铝,A为Fe的氧化物,Y(Fe)与试剂2(硫酸)反应得到E为硫酸亚铁,A与试剂2(硫酸)反应得到D,且D能与Fe反应得到E,则A为氧化铁,D为硫酸铁.Al、氧化铝都与试剂1(NaOH溶液)反应得到C,则C为偏铝酸钠,据此解答.
解答:
解:元素X、Y的单质是生活中常见的金属,分别为Al、Fe中的一种,且X与氧化物A反应得到Y与氧化物B,则X为Al,Y为Fe,B为氧化铝,A为Fe的氧化物,Y(Fe)与试剂2(硫酸)反应得到E为硫酸亚铁,A与试剂2(硫酸)反应得到D,且D能与Fe反应得到E,则A为氧化铁,D为硫酸铁.Al、氧化铝都与试剂1(NaOH溶液)反应得到C,则C为偏铝酸钠,
(1)由上述分析可知,A为Fe2O3,C为NaAlO2,Y为Fe,D为Fe2(SO4)3,
故答案为:Fe2O3;NaAlO2;Fe;Fe2(SO4)3;
(2)D为硫酸铁,检验铁离子的方法为:取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+,
故答案为:取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+;
(3)硫酸铁溶液中Fe3+水解:Fe3++3H2O?Fe(OH)3+3H+,破坏水的电离平衡,溶液呈酸性,
故答案为:Fe3++3H2O?Fe(OH)3+3H+.
(1)由上述分析可知,A为Fe2O3,C为NaAlO2,Y为Fe,D为Fe2(SO4)3,
故答案为:Fe2O3;NaAlO2;Fe;Fe2(SO4)3;
(2)D为硫酸铁,检验铁离子的方法为:取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+,
故答案为:取少量溶液于试管中,滴加几滴KSCN溶液,溶液变红色,则证明原溶液中含有Fe3+;
(3)硫酸铁溶液中Fe3+水解:Fe3++3H2O?Fe(OH)3+3H+,破坏水的电离平衡,溶液呈酸性,
故答案为:Fe3++3H2O?Fe(OH)3+3H+.
点评:本题考查无机物的推断,涉及Fe、Al元素单质化合物的性质,注意对铝热反应的掌握,在推断中经常涉及,难度中等.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案
相关题目
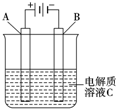
 我国预计在2020年前后建成自己的载人空间站.为了实现空间站的零排放,循环利用人体呼出的CO2并提供氧气.我国科学家设计了一种装置(如图所示),实现“太阳能一电能一化学能”转化,总反应为2CO2=2CO+O2.下列有关说法正确的是( )
我国预计在2020年前后建成自己的载人空间站.为了实现空间站的零排放,循环利用人体呼出的CO2并提供氧气.我国科学家设计了一种装置(如图所示),实现“太阳能一电能一化学能”转化,总反应为2CO2=2CO+O2.下列有关说法正确的是( )| A、该装置属于原电池 |
| B、X极反应式:O2+2H2O+4e-=4OH- |
| C、反应完毕,该太阳能装置中的电解质溶液碱性增强 |
| D、人体呼出的水蒸气参与Y极反应:CO2+H2O+2e-=CO+2OH- |
下列叙述正确的是( )
| A、浓度和体积相同的FeBr2、FeI2溶液中,分别通入少量氯气后都首先发生置换反应 |
| B、XCl3的溶液能与铜片发生反应,则铜的金属性一定比X强 |
| C、非金属X能将Fe氧化到+3价,但非金属Y不能,则Y的氧化性一定比X强 |
| D、Cl2和SO2等体积充分混合后,通入品红溶液,溶液颜色没有明显变化 |
 肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均生成氮气和水,可作火箭燃料.
肼(N2H4)又称联氨,是一种可燃性液体,与氧气或氮氧化物反应均生成氮气和水,可作火箭燃料. (Ⅰ)几种含硅元素的物质之间的相互转化关系如图所示.(注意:在溶液中观察到硅酸沉淀实际上是H4SiO4,H4SiO4在空气中易失水形成H2SiO3)试判断:
(Ⅰ)几种含硅元素的物质之间的相互转化关系如图所示.(注意:在溶液中观察到硅酸沉淀实际上是H4SiO4,H4SiO4在空气中易失水形成H2SiO3)试判断: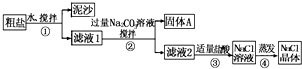
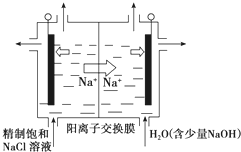 二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.