题目内容
5.下列离子方程式中,正确的是( )| A. | 碳酸钙与盐酸混合 2H++CO32-═CO2↑+H2O | |
| B. | 向氯化铁溶液中加入铁粉 Fe3++Fe═2Fe2+ | |
| C. | 亚硫酸钠溶液与稀硫酸混合 2H++SO32-═SO2↑+H2O | |
| D. | 二氧化锰与浓盐酸混合后加热 MnO2+4H++4Cl-═MnCl2+Cl2↑+2H2O |
分析 A.碳酸钙为沉淀,应保留化学式;
B.电荷不守恒;
C.二者反应生成二氧化硫和水、硫酸钠;
D.氯化锰为可溶性盐,应拆成离子形式.
解答 解:A.碳酸钙与盐酸混合,离子方程式:2H++CaCO3═CO2↑+H2O+Ca2+,故A错误;
B.向氯化铁溶液中加入铁粉,离子方程式:2Fe3++Fe═3Fe2+,故B错误;
C.亚硫酸钠溶液与稀硫酸混合,离子方程式:2H++SO32-═SO2↑+H2O,故C正确;
D.二氧化锰与浓盐酸混合后加热,离子方程式:MnO2+4H++2Cl-═Mn2++Cl2↑+2H2O,故D错误;
故选:C.
点评 本题考查了离子方程式的书写,明确反应实质是解题关键,注意化学式的拆分、电荷的守恒,题目难度不大.

练习册系列答案
相关题目
15.下列说法正确的是( )
| A. | 在 101kPa 下,1克物质燃烧所放出的热量叫做该物质的热值 | |
| B. | 金属的防腐处理中,牺牲阳极的阴极保护法是电解池原理的应用 | |
| C. | 活化分子间的碰撞就是有效碰撞 | |
| D. | 催化剂能增大单位体积内活化分子百分数,从而增大反应速率 |
16.NA表示阿伏加德罗常数,下列说法中正确的是( )
| A. | 常温常压下,48gO2跟48gO3 含有的氧原子数均为3NA | |
| B. | 1L 0.5mol/L的(NH4)2SO4溶液中含有NH4+数目为NA | |
| C. | 标准状况下,11.2L 氨气所含有的原子数是4NA | |
| D. | 80gNaOH溶解在1 L水中,得到溶液的物质的量浓度为2mol/L |
13.将l0mL 0.1mol/L的氨水与6mL 0.2mol/L的盐酸混合后,溶液中各种离子的物质的量浓度由大到小的顺序是( )
| A. | c (Cl-)>c (NH4+)>c (OH-)>c (H+) | B. | c (Cl-)>c (NH4+)>c (H+)>c (OH-) | ||
| C. | c (H+)>c (OH-)>c (Cl-)>c (NH4+) | D. | c (H+)>c (Cl-)>c (NH4+)>c (OH-) |
20.下列叙述正确的是( )
| A. | 原子晶体中只存在非极性共价键 | |
| B. | 干冰升华时,分子内共价键会发生断裂 | |
| C. | 由原子构成的晶体可以是原子晶体,也可以是分子晶体 | |
| D. | 只要含有金属阳离子的晶体就一定是离子晶体 |
17.下列说法正确的是( )
| A. | 含金属元素的离子不一定是阳离子 | |
| B. | 金属单质跟酸反应,一定放出氢气 | |
| C. | 元素从化合态变为游离态时,一定被氧化 | |
| D. | 元素从化合态变为游离态时,一定被还原 |
14.能在水溶液里大量共存,且加入强碱后无显著现象,再加入稀硫酸后既出现沉淀又逸出气体的离子组是( )
| A. | K+、Na+、Al3+、Br- | B. | Na+、K+、SiO32-、CO32- | ||
| C. | Ca2+、Mg2+、NO3-、Cl- | D. | K+、NH4+、AlO2-、Cl- |
15.ZnC2、Al4C3、Mg2C3、Li2C2等与CaC2和H2O反应相似.下列说法不正确的是( )
| A. | C22-的电子式是[ ]2- ]2- | |
| B. | Mg2C3和Li2C2与水反应生成的烃可能具有相同的官能团 | |
| C. | 1mol ZnC2与水反应生成的烃的体积约为22.4L | |
| D. | Al4C3与水反应生成的烃分子中只有极性键 |
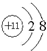 ;与E同周期的元素中,金属性最弱的金属元素名称是铝,所形成的最稳定的气态氢化物的化学式为HCl;
;与E同周期的元素中,金属性最弱的金属元素名称是铝,所形成的最稳定的气态氢化物的化学式为HCl;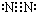 ,B与D通常能形成分子晶体,在E2D2中含有的化学键有离子键、共价键;
,B与D通常能形成分子晶体,在E2D2中含有的化学键有离子键、共价键;