题目内容
17.下列有关化学用语或名称表达正确的是( )| A. | 聚丙烯的结构简式: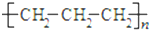 | |
| B. | 乙炔的分子结构模型示意图: | |
| C. | H2O2的电子式:H+[${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$$\underset{\stackrel{••}{O}}{••}$${\;}_{•}^{•}$]2-H+ | |
| D. |  的名称:3-甲基-1-丁醇 的名称:3-甲基-1-丁醇 |
分析 A.聚丙烯的主链只有2个C;
B.乙炔分子中存在碳碳三键,为直线型结构;
C.过氧化氢为共价化合物,分子中不存在阴阳离子;
D.该有机物为醇,根据醇的命名原则判断.
解答 解:A.聚丙烯为丙烯的加聚反应产物,聚丙烯正确的结构简式为: ,故A错误;
,故A错误;
B.乙炔为直线型结构,乙炔正确的比例模型为: ,故B错误;
,故B错误;
C.过氧化氢属于共价化合物,其正确的电子式为: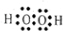 ,故C错误;
,故C错误;
D. 中羟基位于1号C,在3号C含有1个甲基,该有机物名称为:3-甲基-1-丁醇,故D正确;
中羟基位于1号C,在3号C含有1个甲基,该有机物名称为:3-甲基-1-丁醇,故D正确;
故选D.
点评 本题考查化学用语的书写判断,题目难度中等,涉及结构简式、结构示意图、电子式等,把握化学用语的区别及规范应用为解答的关键,注重基础知识的考查.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8. 当今世界,能源的发展日益成为全世界、全人类共同关心的问题.
当今世界,能源的发展日益成为全世界、全人类共同关心的问题.
(1)A和B的单质单位质量的燃烧热大,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如表所示:
①请根据上述信息,写出A的核外电子排布式:1s22s2.
②某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了能量最低原理.
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.
①已知金刚石中碳碳键的键长为154.45pm,C60中碳碳键的键长为145pm和140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由否或不正确,理由:C60是分子晶体,金刚石是原子晶体,熔化时C60破坏分子间作用力而金刚石破坏共价键,所以C60的沸点低于金刚石.
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.
③继C60后,科学家又合成Si60、N60,请比较C、Si、N原子电负性由大到小的顺序N>C>Si.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则一个Si60分子中所含π键的数目为30.
 当今世界,能源的发展日益成为全世界、全人类共同关心的问题.
当今世界,能源的发展日益成为全世界、全人类共同关心的问题.(1)A和B的单质单位质量的燃烧热大,可用作燃料.已知A和B为短周期元素,其原子的第一至第四电离能如表所示:
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 899 | 1 757 | 14 840 | 21 000 |
| B | 738 | 1 451 | 7 733 | 10 540 |
②某同学根据上述信息,推断B的核外电子排布如图1所示,该同学所画的电子排布图违背了能量最低原理.
(2)氢气作为一种清洁能源,必须解决它的储存问题,C60可用作储氢材料.
①已知金刚石中碳碳键的键长为154.45pm,C60中碳碳键的键长为145pm和140pm,有同学据此认为C60的熔点高于金刚石,你认为是否正确并阐述理由否或不正确,理由:C60是分子晶体,金刚石是原子晶体,熔化时C60破坏分子间作用力而金刚石破坏共价键,所以C60的沸点低于金刚石.
②科学家把C60和K掺杂在一起制造了一种富勒烯化合物,其晶胞如图2所示,该物质在低温时是一种超导体.该物质中K原子和C60分子的个数比为3:1.
③继C60后,科学家又合成Si60、N60,请比较C、Si、N原子电负性由大到小的顺序N>C>Si.Si60分子中每个硅原子只跟相邻的3个硅原子形成共价键,且每个硅原子最外层都满足8电子稳定结构,则一个Si60分子中所含π键的数目为30.
5.对表中有关离子方程式书写评价合理的是( )
| 选项 | 化学反应及其离子方程式 | 评价 |
| A | Fe3O4与过量稀硝酸反应:Fe3O4+8H+→2Fe3++Fe2++4H2O | 正确 |
| B | 在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液: 2Fe3++3SO42-+3Ba2++6OH-→3BaSO4↓+2Fe(OH)3↓ | 正确 |
| C | 在稀氨水中通入过量CO2:NH3•H2O+CO2→NH4++HCO3- | 正确 |
| D | FeBr2溶液与等物质的量的Cl2反应: 2Fe2++2Br-+2Cl2→2Fe3++4Cl-+Br2 | 错误,Fe2+与Br-的化学计量数之比应为1:2 |
| A. | A | B. | B | C. | C | D. | D |
12.X、Y、Z、W四种短周期元素在元素周期表中的相对位置如表所示,Z的单质是常见的半导体材料.下列说法正确的是( )
| X | ||
| Y | Z | W |
| A. | X、Z、W的简单氢化物的稳定性Z>W>X | |
| B. | X元素的单质在化学反应中只表现还原性 | |
| C. | X、Y的简单离子半径Y>X | |
| D. | Y、Z、X的最高价氧化物均能与NaOH溶液反应 |
2.Fenton试剂常用于氧化降解有机污染物X.在一定条件下,反应初始时c(X)=2.0×10-3 mol•L-1,反应10min进行测定,得图1和图2.下列说法不正确的是( )
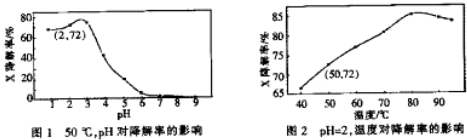

| A. | 温度为50℃,pH在3~6之间,X降解率随pH增大而减小 | |
| B. | pH=2,温度在40~80℃,X降解率温度升高而增大 | |
| C. | 无需再进行后续实验,就可以判断最佳反应条件是:pH=3、温度为80℃ | |
| D. | pH=2,温度为50℃,10min内v(X)=1.44×10-4 mol•L-1 min-1 |
9.A、B、C、D、E是中学化学中五种常见元素,有关信息如表:
请回答下列问题:
(1)A的氢化物分子式是NH3,其水溶液能使酚酞变红的原因(用电离方程式解释)为:NH3•H2O?NH4++OH-;
(2)A、D的氢化物相互反应,产生大量白烟,该反应的方程式为:NH3+HCl=NH4Cl;
(3)A与B可组成质量比为7:16的三原子分子,该分子的化学式为NO2.
| 元素 | 有关信息 |
| A | 其氢化物水溶液呈碱性 |
| B | 地壳中含量最多的元素 |
| C | 单质须保存在煤油中 |
| D | 单质与NaOH溶液反应可用于生产漂白液 |
| E | 单质是生活中用量最大的金属,其制品在潮湿空气中易被腐蚀或损坏 |
(1)A的氢化物分子式是NH3,其水溶液能使酚酞变红的原因(用电离方程式解释)为:NH3•H2O?NH4++OH-;
(2)A、D的氢化物相互反应,产生大量白烟,该反应的方程式为:NH3+HCl=NH4Cl;
(3)A与B可组成质量比为7:16的三原子分子,该分子的化学式为NO2.
7.消除氮氧化物和硫氧化物有多种方法.
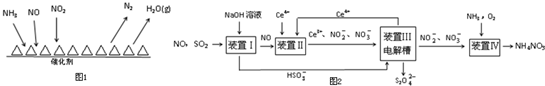
Ⅰ.NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图1所示:
①由图可知SCR技术中的氧化剂为NO、NO2.
②用Fe做催化剂时,在氨气足量的情况下,当$\frac{c(N{O}_{2})}{c(NO)}$=1:1时,脱氮率最佳,已知每生成28g N2 放出的热量为QkJ,该反应的热化学方程式为2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-2QkJ/mol.
Ⅱ.工业上变“废”为宝,吸收工业中SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如图2(Ce为铈元素):
①装置Ⅰ中的主要反应的离子方程式为SO2+OH-=HSO3-.
②装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1mol CH4时,理论上可再生8mol Ce4+.
Ⅲ.用活性炭还原法可以处理氮氧化物.如发生反应:C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ/mol.
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
①Tl℃时,该反应的平衡常数K=$\frac{9}{16}$.
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是通入一定量的NO或适当缩小容器的体积或增大压强或通入等物质的量的CO2和N2(答一种即可).
Ⅰ.NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术.反应原理如图1所示:
①由图可知SCR技术中的氧化剂为NO、NO2.
②用Fe做催化剂时,在氨气足量的情况下,当$\frac{c(N{O}_{2})}{c(NO)}$=1:1时,脱氮率最佳,已知每生成28g N2 放出的热量为QkJ,该反应的热化学方程式为2NH3(g)+NO(g)+NO2(g)?2N2(g)+3H2O(g)△H=-2QkJ/mol.
Ⅱ.工业上变“废”为宝,吸收工业中SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如图2(Ce为铈元素):
①装置Ⅰ中的主要反应的离子方程式为SO2+OH-=HSO3-.
②装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1mol CH4时,理论上可再生8mol Ce4+.
Ⅲ.用活性炭还原法可以处理氮氧化物.如发生反应:C(s)+2NO(g)?N2(g)+CO2(g)△H=Q kJ/mol.
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间(min) 浓度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是通入一定量的NO或适当缩小容器的体积或增大压强或通入等物质的量的CO2和N2(答一种即可).

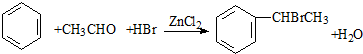 (卤烷基化反应)
(卤烷基化反应)
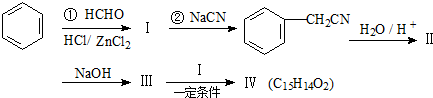
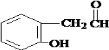 ,
,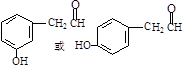 .
.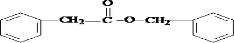 .
.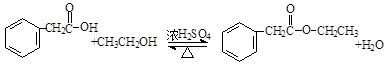 .
.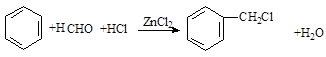 .
.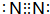 .
.