题目内容
有一块表面氧化成氧化钠的金属钠,质量是5.4g,将它投入到100g水中完全反应后,收集到标况下1.12L的气体,试计算:
(1)未被氧化的金属钠的质量是多少克?
(2)被氧化成氧化钠的金属钠的质量是多少克?
(3)反应后所得溶液的物质的量浓度是多少?(假设溶液的体积不变)
(1)未被氧化的金属钠的质量是多少克?
(2)被氧化成氧化钠的金属钠的质量是多少克?
(3)反应后所得溶液的物质的量浓度是多少?(假设溶液的体积不变)
考点:化学方程式的有关计算,有关混合物反应的计算
专题:计算题
分析:(1)计算氢气的物质的量,根据反应2Na+2H2O=2NaOH+H2↑计算样品中Na的物质的量,再根据m=nM计算Na的质量;
(2)根据(1)中的Na的质量可计算氧化钠的质量,根据氧化钠中Na元素质量分数计算被氧化成氧化钠的金属钠的质量;
(3)根据(1)(2)中所求可计算Na元素的质量,利用n=
计算其物质的量,再利用钠元素守恒计算生成NaOH的总物质的量,根据c=
计算溶液物质的量浓度.
(2)根据(1)中的Na的质量可计算氧化钠的质量,根据氧化钠中Na元素质量分数计算被氧化成氧化钠的金属钠的质量;
(3)根据(1)(2)中所求可计算Na元素的质量,利用n=
| m |
| M |
| n |
| V |
解答:
解:(1)n(H2)=
=0.05mol
由2Na+2H2O=2NaOH+H2↑可知,n(Na)=2n(H2)=2×0.05mol=0.1mol
未被氧化的金属钠的质量是:m(Na)=0.1mol×23g/mol=2.3g
答:未被氧化的金属钠的质量为2.3g.
(2)m(Na2O)=5.4g-2.3g=3.1g,则被氧化成氧化钠的金属钠的质量=3.1g×
=2.3g,
答:被氧化成氧化钠的金属钠的质量为2.3;
(3)混合物中n(Na元素)=
=0.2mol,则与水反应生成的总NaOH的物质的量为:n(NaOH)=0.2mol,溶液的体积既水的体积:100g÷1g/mL=100mL
c(NaOH)=0.2mol÷0.100L=2mol/L
答:所得溶液的物质的量浓度为2mol/L.
| 1.12L |
| 22.4L/mol |
由2Na+2H2O=2NaOH+H2↑可知,n(Na)=2n(H2)=2×0.05mol=0.1mol
未被氧化的金属钠的质量是:m(Na)=0.1mol×23g/mol=2.3g
答:未被氧化的金属钠的质量为2.3g.
(2)m(Na2O)=5.4g-2.3g=3.1g,则被氧化成氧化钠的金属钠的质量=3.1g×
| 46 |
| 62 |
答:被氧化成氧化钠的金属钠的质量为2.3;
(3)混合物中n(Na元素)=
| 2.3g+2.3g |
| 23g/mol |
c(NaOH)=0.2mol÷0.100L=2mol/L
答:所得溶液的物质的量浓度为2mol/L.
点评:本题考查钠元素单质化合物性质、根据方程式计算,根据氢气的质量计算氧化钠的质量为解答该题的关键,难度中等.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案 名校联盟快乐课堂系列答案
名校联盟快乐课堂系列答案
相关题目
用加热的方法可以分离的一组物质是( )
| A、氯化铵和消石灰 |
| B、碳酸氢钠和氯化铵 |
| C、碳酸氢铵和过氧化钠 |
| D、氯化铵和氯化钠 |
下列各组物质中,第一种是酸,第二种是混合物,第三种是碱的是( )
| A、氧化铁、硫酸铜、硫酸 |
| B、氢氟酸、空气、纯碱 |
| C、硝酸、胆矾、熟石灰 |
| D、醋酸、食盐水、烧碱 |
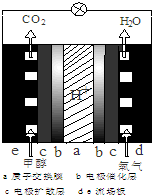 以甲醇为替代燃料是解决我国石油资源短缺的重要措施.
以甲醇为替代燃料是解决我国石油资源短缺的重要措施.