题目内容
【题目】A、B是中学化学常见的化合物,它们各由两种元素组成;乙为元素R组成的单质,它们之间存在如图所示关系.根据要求回答问题:
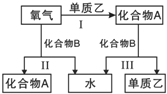
![]() 如图三个反应中,属于氧化还原反应的有______个.
如图三个反应中,属于氧化还原反应的有______个.
![]() 若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有______.
若元素R与氧同主族,下列事实能说明R与氧的非金属性相对强弱的有______.
A.还原性:![]() B.酸性:
B.酸性:![]()
C.稳定性:![]() C.沸点:
C.沸点:![]()
![]() 若化合物B常温下为气体,其水溶液呈碱性
若化合物B常温下为气体,其水溶液呈碱性![]() 答题必须用具体物质表示
答题必须用具体物质表示![]() .
.
![]() 化合物B的电子式为______;其水溶液呈碱性的原因是______
化合物B的电子式为______;其水溶液呈碱性的原因是______![]() 用离子方程式表示
用离子方程式表示![]() .
.
![]() 化合物B可与
化合物B可与![]() 组成燃料电池
组成燃料电池![]() 氢氧化钾溶液为电解质溶液
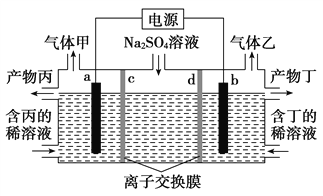
氢氧化钾溶液为电解质溶液![]() ,其反应产物与反应Ⅲ相同.写出该电池负极的电极反应式______.
,其反应产物与反应Ⅲ相同.写出该电池负极的电极反应式______.
![]() 当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为
当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为![]() 和
和![]() ,则反应Ⅰ的热化学方程式为______
,则反应Ⅰ的热化学方程式为______![]() 注:反应条件相同、所有物质均为气体
注:反应条件相同、所有物质均为气体![]() .
.
【答案】3 A、C ![]()
![]()
![]()
![]()
![]()
![]()
【解析】
![]() 、B是中学化学常见的化合物,它们各由两种元素组成,乙为元素R组成的单质,反应Ⅰ、Ⅱ为有氧气参加的反应,应为氧化还原反应,反应Ⅲ由化合物A、B反应生成单质,也应为氧化还原反应;
、B是中学化学常见的化合物,它们各由两种元素组成,乙为元素R组成的单质,反应Ⅰ、Ⅱ为有氧气参加的反应,应为氧化还原反应,反应Ⅲ由化合物A、B反应生成单质,也应为氧化还原反应;
![]() 元素R与氧同主族,则R为硫元素,硫的非金属性弱于氧,根据元素周期律判断;
元素R与氧同主族,则R为硫元素,硫的非金属性弱于氧,根据元素周期律判断;
![]() 若化合物B常温下为气体,其水溶液呈碱性,则B为
若化合物B常温下为气体,其水溶液呈碱性,则B为![]() ,根据转化关系可知,A为NO,乙为
,根据转化关系可知,A为NO,乙为![]() ,据此答题。
,据此答题。
![]() 、B是中学化学常见的化合物,它们各由两种元素组成,乙为元素R组成的单质,反应Ⅰ、Ⅱ为有氧气参加的反应,应为氧化还原反应,反应Ⅲ由化合物A、B反应生成单质,也应为氧化还原反应,所以属于氧化还原反应的有Ⅰ、Ⅱ、Ⅲ,共3个;
、B是中学化学常见的化合物,它们各由两种元素组成,乙为元素R组成的单质,反应Ⅰ、Ⅱ为有氧气参加的反应,应为氧化还原反应,反应Ⅲ由化合物A、B反应生成单质,也应为氧化还原反应,所以属于氧化还原反应的有Ⅰ、Ⅱ、Ⅲ,共3个;
![]() 元素R与氧同主族,则R为硫元素,硫的非金属性弱于氧,根据元素周期律可知,能说明S与氧的非金属性相对强弱的有,还原性:
元素R与氧同主族,则R为硫元素,硫的非金属性弱于氧,根据元素周期律可知,能说明S与氧的非金属性相对强弱的有,还原性:![]() 、稳定性:
、稳定性:![]() ,故答案为:A、C;
,故答案为:A、C;
![]() 若化合物B常温下为气体,其水溶液呈碱性,则B为
若化合物B常温下为气体,其水溶液呈碱性,则B为![]() ,根据转化关系可知,A为NO,乙为
,根据转化关系可知,A为NO,乙为![]() ;
;
![]() 化合物B的电子式为
化合物B的电子式为![]() ;其水溶液呈碱性的原因是一水合氨电离产生氢氧根离子,离子方程式为
;其水溶液呈碱性的原因是一水合氨电离产生氢氧根离子,离子方程式为![]()
![]()
![]() ;
;
![]() 化合物
化合物![]() 与
与![]() 组成燃料电池
组成燃料电池![]() 氢氧化钾溶液为电解质溶液
氢氧化钾溶液为电解质溶液![]() ,电池负极为氨气发生氧化反应生成氮气和水,电极反应式为
,电池负极为氨气发生氧化反应生成氮气和水,电极反应式为![]() ;
;
![]() 当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为
当1mol的化合物B分别参与反应Ⅱ、Ⅲ时,热效应为![]() 和
和![]() ,根据盖斯定律,将反应反应
,根据盖斯定律,将反应反应![]() Ⅰ
Ⅰ![]() Ⅱ
Ⅱ![]() 可得反应Ⅰ的热化学方程式为
可得反应Ⅰ的热化学方程式为![]() 。
。

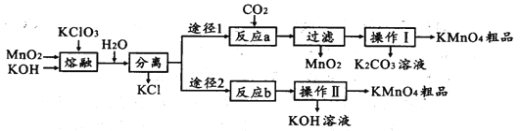
【题目】苯甲酸是一种消毒防腐剂,其钠盐可抑制牙膏中微生物的生长。甲苯氧化法是实验室制备苯甲酸的常用方法之一。
(一)反应原理
C6H5CH3+2KMnO4![]() C6H5COOK+KOH+2MnO2↓+H2O
C6H5COOK+KOH+2MnO2↓+H2O
C6H5COOK+HCl→C6H5COOH+KCl
已知:苯甲酸相对分子质量122,熔点122.4℃;苯甲酸在水中的溶解度如下表。
温度/℃ | 17.5 | 25 | 75 | 80 | 100 |
溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 |
(二)实验过程
①将一定量甲苯、水、几粒沸石加入三颈烧瓶中;
②装上冷凝管,加热至沸后分批加入适量高锰酸钾,搅拌回流反应4小时;
③将反应混合物趁热减压过滤,并用热水洗涤滤渣,将洗涤液并入滤液中;
④滤液加入盐酸酸化后,抽滤(装置如图1)、洗涤、干燥得苯甲酸粗产品。
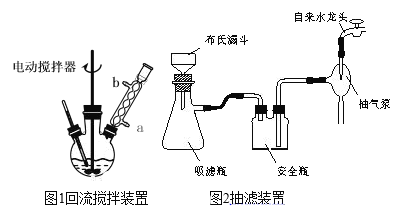
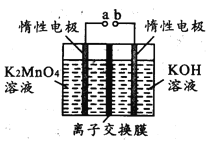
(1)图1电动搅拌器的作用是_____,冷凝管中冷水应从_____(填“a”或“b”)口进入;判断甲苯被氧化完全的实验现象是____。
(2)第③步抽滤操作时,要趁热进行,是因为_____,反应混合物趁热减压过滤后,若溶液呈红色,可用少量NaHSO3溶液处理,反应的离子方程式为_____。
(三)纯度测定
(3)称取1.22g产品溶解在甲醇中配成100mL溶液,移取25.00mL溶液,用KOH标准溶液进行滴定,消耗KOH的物质的量为2.30×10-3mol,产品中苯甲酸质量百分数为____(保留两位有效数字)。
(四)实验反思
(4)得到的粗产品要进一步提纯苯甲酸,可采用_____的方法。