题目内容
【题目】氟及其化合物用途非常广泛。回答下列问题:
(1)基态锑(Sb)原子价电子排布的轨道式为____。[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,该离子的空间构型为______,依次写出一种与[H2F]+具有相同空间构型和键合形式的分子和阴离子分别是_______、_________。
(2)硼酸(H3BO3)和四氟硼酸铵(NH4BF4)都有着重要的化工用途。
①H3BO3和NH4BF4涉及的四种元素中第二周期元素的第一电离能由大到小的顺序_____(填元素符号)。
②H3BO3本身不能电离出H+,在水中易结合一个OH﹣生成[B(OH)4]﹣,而体现弱酸性。[B(OH)4]﹣中B原子的杂化类型为_____。
③NH4BF4(四氟硼酸铵)可用作铝或铜焊接助熔剂、能腐蚀玻璃等。四氟硼酸铵中存在_______(填序号):
A 离子键 B σ键 C π键 D 配位键 E 范德华力
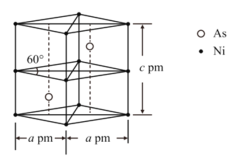
(3)某砷镍合金的晶胞如图所示,设阿伏加德罗常数的值为![]() ,该晶体的密度ρ_________g·cm-3。
,该晶体的密度ρ_________g·cm-3。
 。
。
【答案】![]() V形 H2O NH2 F>N>O>B sp3 ABD
V形 H2O NH2 F>N>O>B sp3 ABD ![]()
【解析】
(1)根据锑元素原子核外电子排布写出基态锑(Sb)原子价电子排布的轨道式;用价层电子对互斥理论判断[H2F]+的空间构型;用替代法书写与[H2F]+具有相同空间构型和键合形式的分子和阴离子;
(2)①同周期主族元素自左而右原子半径减小,第一电离能呈增大趋势;
②[B(OH)4]﹣中B的价层电子对=4+![]() (3+1-4×1) =4,所以采取sp3杂化;
(3+1-4×1) =4,所以采取sp3杂化;
③NH4BF4 (四氟硼酸铵)中含铵根离子和氟硼酸根离子,二者以离子键相结合;铵根离子中含3个σ键和1个配位键,氟硼酸根离子中含3个σ键和1个配位键;
(3)由晶胞结构可知,每个晶胞中含有2个Ni原子和2个As原子,计算晶胞的质量,晶胞的密度=![]() ;
;
(1)锑为51号元素,Sb 位于第五周期VA族,则基态锑(Sb)原子价电子排布的轨道式为![]() ;[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,[H2F]+中中心原子F的价层电子对数为2+
;[H2F]+[SbF6]—(氟酸锑)是一种超强酸,存在[H2F]+,[H2F]+中中心原子F的价层电子对数为2+![]() =4,σ键电子对数为2,该离子的空间构型为V型,与[H2F]+具有相同空间构型和键合形式的分子为H2O、阴离子为NH2,
=4,σ键电子对数为2,该离子的空间构型为V型,与[H2F]+具有相同空间构型和键合形式的分子为H2O、阴离子为NH2,
故答案为:![]() ;V形; H2O;NH2;
;V形; H2O;NH2;
(2)①H3BO3和NH4BF4涉及的四种元素中第二周期元素是B、N、O、F四种元素,同周期元素从左向右第一电离能呈增大趋势,N的2p能级半充满较稳定,N的第一电离能大于O,则这四种元素第一电离能由大到小的顺序为F>N>O>B,
故答案为: F>N>O>B;
②[B(OH)4]﹣中B的价层电子对=4+![]() (3+1-4×1) =4,所以采取sp3杂化,
(3+1-4×1) =4,所以采取sp3杂化,
故答案为:sp3;
③NH4BF4 (四氟硼酸铵)中含铵根离子和氟硼酸根离子,二者以离子键相结合;铵根离子中含3个σ键和1个配位键,氟硼酸根离子中含3个σ键和1个配位键,铵根离子和氟硼酸根离子以离子键相结合,则四氟硼酸铵中存在离子键、σ键、配位键,
故答案为:ABD;
(3)由晶胞结构可知,每个晶胞中含有Ni原子数目=8×![]() +4×
+4×![]() =2,含有2个As原子,晶胞的质量=2×
=2,含有2个As原子,晶胞的质量=2×![]() g,晶胞的体积V=a×10-10cm×a×10-10cm×
g,晶胞的体积V=a×10-10cm×a×10-10cm×![]() ×c×10-10cm=
×c×10-10cm=![]() ×10-30cm3,故晶胞的密度ρ=
×10-30cm3,故晶胞的密度ρ= g·cm-3,
g·cm-3,
故答案为:![]() 。
。

 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案 金版课堂课时训练系列答案
金版课堂课时训练系列答案 单元全能练考卷系列答案
单元全能练考卷系列答案【题目】W、X、Y、Z、M、R为6种短周期元素。W原子的核电荷数等于其周期数,X+与Ne具有相同的电子层结构,Y原子与Z原子的最外层电子数之和与R原子的最外层电子数相等;Y、Z、M、R在周期表中的相对位置如图所示。
Z | M | R | ||
Y |
(1)Z元素在周期表的位置为________。
(2)R离子的结构示意图为_________。
(3)X与M以1:1形成的化合物中存在的化学键类型为____________。
(4)Y的最高价氧化物与X的最高价氧化物的水化物在水溶液中发生反应的离子方程式为_________________________________。
(5)Y与Z 形成相对分子量为144的化合物与M的简单氢化物反应,生成最简单的烃和Y的最高价氧化物的水化物,该反应的化学方程式为__________________________。
(6)M与R可形成M2R2分子,该分子中各原子均达到8电子稳定结构,则M2R2的电子式为__________________。