题目内容
5.下列有关实验的现象与对应结论均正确的是 ( )| 选项 | 实验 | 现象 | 结论 |
| A | 铜片加入浓硝酸中 | 产生红棕色气体 | 浓硝酸具有强氧化性 |
| B | 将一小块钠放入乙醇中 | 产生大量气泡 | 该乙醇中含有较多水 |
| C | 向CuSO4溶液中通入H2S气体 | 出现黑色沉淀 | H2S的酸性比H2SO4强 |
| D | 向AgCl悬浊液中滴加KI溶液 | 白色沉淀变黄色 | AgI的溶解度大于AgCl |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Cu性质较不活泼,能被强氧化剂氧化;
B.钠性质较活泼,能和醇中羟基发生反应生成氢气;
C.硫酸铜和硫化氢发生复分解反应生成硫化铜沉淀,同时生成硫酸,硫酸是强电解质、氢硫酸是弱电解质;
D.溶度积常数大的物质能转化为溶度积常数小的物质.
解答 解:A.Cu性质较不活泼,能被强氧化剂氧化,铜和浓硝酸反应生成红棕色气体二氧化氮,说明铜被硝酸氧化,则硝酸体现强氧化性,故A正确;
B.钠性质较活泼,能和醇中羟基发生反应生成氢气,所以不能说明乙醇中含有水,故B错误;
C.硫酸铜和硫化氢发生复分解反应生成硫化铜沉淀,同时生成硫酸,硫酸是强电解质、氢硫酸是弱电解质,所以硫酸酸性大于氢硫酸,故C错误;
D.溶度积常数大的物质能转化为溶度积常数小的物质,向AgCl悬浊液中滴加KI溶液,白色沉淀转化为黄色,说明AI的溶度积小于AgCl,二者结构相似,溶度积越大其溶解度越大,所以AI的溶解度小于AgCl,故D错误;
故选A.
点评 本题考查物质性质、溶度积常数等知识点,侧重考查基本理论,易错选项是C,注意:一般来说强酸能制取弱酸,但硫酸铜和硫化氢反应生成硫酸违反这一规律,为易错点.

练习册系列答案
 通城学典默写能手系列答案
通城学典默写能手系列答案 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目
16.下列溶液中,有关物质的量浓度关系正确的是( )
| A. | 向硝酸钠溶液中滴加稀盐酸得到的pH=5的混合溶液:c(Na+ )=c(NO3 - ) | |
| B. | 1.0 mol•L-1Na2CO3 溶液:c(OH-)=c(HCO3-)+c(H+) | |
| C. | pH=8.0的KHS溶液中,c(K+)>c(HS-)>c(OH-)>c(S2-)>c(H+) | |
| D. | 将0.2 mol•L-1的某一元酸HA溶液和0.1 mol•L-1NaOH溶液等体积混合后,溶液pH大于7,则反应后的混合液中:2c(OH-)+c (A-)=2c(H+)+c(HA) |
13.新型纳米材料MFe2Ox(3<x<4)中M表示+2价的金属元素,在反应中M化合价不发生变化.常温下,MFe2Ox能使工业废气中的(SO2)转化为S,流程如下:MFe2Ox$→_{常温}^{SO_{2}}$MFe2Oy下列判断正确的是( )
| A. | SO2是该反应的催化剂 | B. | MFe2Ox是还原剂 | ||
| C. | X<Y | D. | SO2发生了置换反应 |
20.近年来,乳酸成为研究热点之一,以乳酸为原料制成的高分子材料具有生物兼容性.已知乳酸的结构简式为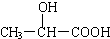 ,下列物质中能与乳酸反应的是( )
,下列物质中能与乳酸反应的是( )
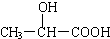 ,下列物质中能与乳酸反应的是( )
,下列物质中能与乳酸反应的是( )| A. | 金属铁 | B. | NH4Cl溶液 | C. | 乙烷 | D. | 苯 |
8.短周期主族元素X、Y、Z、W的原子序数依次增大,其原子的最外层电子数之和为19.X的简单阴离子比W的简单阴离子少2层电子,Y与Z位于相邻周期,Y、Z的氧化物排放到空气中会形成酸雨.下列说法正确的是( )
| A. | 四种元素中,元素Z的非金属性最强 | |
| B. | X、Y、Z三种元素不可能形成离子化合物 | |
| C. | Y、Z、W三种元素的原子半径大小顺序:r(Z)>r(W)>r(Y) | |
| D. | YW3、ZW2、Z2W2中各原子最外层均达到8电子稳定结构 |
9.把图2的碎纸片补充到图1中,可得到一个完整的氧化还原反应的离子方程式(未配平).下列对该反应的说法不正确的是( )


| A. | IO4作氧化剂 | |
| B. | 若有1molMn2+参加反应转移5mol电子 | |
| C. | 氧化剂与还原剂的物质的量之比为5:2 | |
| D. | 配平后Mn2+、H+的化学计量数分别为2、3 |