题目内容
14.在恒容密闭容器中通入X、Y、Z发生反应:2X(g)?Y(g)+C(s),已知温度T1>T2,X的物质的量浓度c(X)随时间t变化曲线如图甲,速率变化如图乙,下列叙述不正确的是( )
| A. | 如图甲在T2线上,正反应速率:N点>W点 | |
| B. | 如图甲在T2下,在0~t1时间内的平均速率,v(X)=$\frac{a-b}{{t}_{1}}$ mol•L-1•min-1 | |
| C. | 增加C的量,化学反应速率增大 | |
| D. | 如图乙,t0时可能是加入了催化剂 |
分析 A、温度一定时,反应物浓度越小,正反应速率越小;
B、根据图中X的浓度变化求出X的浓度变化,再求反应速率;
C、C是固体,增加C的量但浓度不变;
D、使用催化剂正、逆反应速率都变大,但平衡不移动.
解答 解:A、温度一定时,反应物浓度越小,正反应速率越小,即正反应速率:N点>W点,故A正确;
B、T2下,在0~t1时间内,X的浓度变化为:c(X)=(a-b)mol/L,所以v(X))=$\frac{a-b}{{t}_{1}}$ mol•L-1•min-1,故B正确;
C、C是固体,增加C的量但浓度不变,所以化学反应速率不变,故C错误;
D、使用催化剂正、逆反应速率都变大,但平衡不移动,所以t0时可能是加入了催化剂,故D正确;
故选AC.
点评 本题考查了化学平衡图象问题、平衡有关计算、外界条件对平衡移动影响等,难度中等,根据图象判断反应为放热反应是解题的关键.注意把握图象中曲线的变化特点,分析外界条件对化学平衡的影响.

练习册系列答案
相关题目
5. 如图是某有机物分子的比例模型(填充模型),其中○代表氢原子,
如图是某有机物分子的比例模型(填充模型),其中○代表氢原子, 表示碳原子,
表示碳原子,
 代表氧原子.该有机物的名称是( )
代表氧原子.该有机物的名称是( )
 如图是某有机物分子的比例模型(填充模型),其中○代表氢原子,
如图是某有机物分子的比例模型(填充模型),其中○代表氢原子, 表示碳原子,
表示碳原子, 代表氧原子.该有机物的名称是( )
代表氧原子.该有机物的名称是( )| A. | 乙烷 | B. | 乙烯 | C. | 乙酸 | D. | 乙醇 |
19.某溶液中大量存在以下浓度的五种离子:0.2mol/L Cl-、0.4mol/L SO${\;}_{4}^{2-}$、0.1mol/L Al3+、0.3mol/L H+、M,则M及物质的量浓度(mol/L)可能为( )
| A. | Na+0.3 | B. | Ba2+0.2 | C. | CO${\;}_{3}^{2-}$ 0.2 | D. | Zn2+0.2 |
6.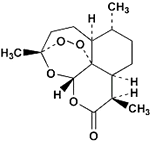 2015年10月5日,中国科学家屠呦呦首次获诺贝尔生理学或医学奖,以表彰她发现了一种药物--青蒿素,它是由菊科植物在低湿条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构简式如图所示.下列有关青蒿素的说法不正确的是( )
2015年10月5日,中国科学家屠呦呦首次获诺贝尔生理学或医学奖,以表彰她发现了一种药物--青蒿素,它是由菊科植物在低湿条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构简式如图所示.下列有关青蒿素的说法不正确的是( )
 2015年10月5日,中国科学家屠呦呦首次获诺贝尔生理学或医学奖,以表彰她发现了一种药物--青蒿素,它是由菊科植物在低湿条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构简式如图所示.下列有关青蒿素的说法不正确的是( )
2015年10月5日,中国科学家屠呦呦首次获诺贝尔生理学或医学奖,以表彰她发现了一种药物--青蒿素,它是由菊科植物在低湿条件下提炼出来的一种化合物,是治疗疟疾的特效药,其结构简式如图所示.下列有关青蒿素的说法不正确的是( )| A. | 青蒿素的分子式为C15H22O5 | |
| B. | 青蒿素不易溶于水,可溶于乙醚 | |
| C. | 青蒿素在一定条件下可发生水解、取代、加成、氧化反应 | |
| D. | 青蒿素分子内的一个过氧基团是对付疟原虫的核心基团 |
3.常温下,醋酸与氢氧化钠发生中和反应,当醋酸过量时,溶液的pH可能为( )
| A. | pH<7 | B. | pH=7 | C. | pH>7 | D. | 都有可能 |
4.一定条件下存在反应:CO(g)+H2O(g)═CO2(g)+H2(g),△H<0.现有三个相同的2L恒容绝热(与外界没有热量交换) 密闭容器I、II、III,在I中充入1mol CO和1mol H2O,在II中充入1mol CO2 和1mol H2,在III中充入2mol CO 和2mol H2O,700℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A. | 容器I、II中正反应速率相同 | |
| B. | 容器I中CO 的物质的量比容器II中的多 | |
| C. | 容器I、III中反应的平衡常数相同 | |
| D. | 容器I中CO 的转化率与容器II中CO2 的转化率之和等于1 |