��Ŀ����
��ӦaA(g)��bB(g) cC(g)(��H<0)�ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯��������ͼ��ʾ��
cC(g)(��H<0)�ڵ��������½��С��ı�������Ӧ�������ڢ����ϵ�и�����Ũ����ʱ��仯��������ͼ��ʾ��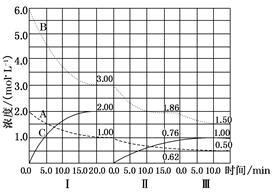
�ش����⣺
(1)B��ƽ��ת���ʦ���(B)������(B)������(B)����С���� ����ֵ�� ��
(2)�ɵ�һ��ƽ��ڶ���ƽ�⣬ƽ���ƶ��ķ����� ����ȡ�Ĵ�ʩ�� ��
(3)�Ƚϵڢ�η�Ӧ�¶�(T2)�͵ڢ�η�Ӧ�¶�(T3)�ĸߵͣ�T2 T3(�>������<����������)���жϵ������� ��
(1)����(B) 0.19(��19%)
(2)������Ӧ���� �ӷ�Ӧ��ϵ���Ƴ�����C
(3)> �˷�ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������Ӧ�����ƶ�
����

 ȫ�ŵ�����Ԫ�ƻ�ϵ�д�
ȫ�ŵ�����Ԫ�ƻ�ϵ�д�������������Ǻ���һ�����һ�������ˮƽ����Ҫ��־��
��1��һ�������£�SO2�������Ӧ10 min��SO2��SO3���ʵ���Ũ�ȷֱ�Ϊ1.2 mol/L��2.0 mol/L����SO2��ʼ���ʵ���Ũ��Ϊ______������SO3�Ļ�ѧ��Ӧ����Ϊ______��
��2�����ı��������������SO2�������Ӧ����SO3��ʹ10 min�ڵ���O2��ʾ�ķ�Ӧ����Ϊ0.15mol/(L��min)����ı������������_______________��
| A��ѹ�����������ѹǿ | B�������¶� | C����������ĵ��� | D��������SO2��Ũ�� |
��16�֣���һ�ݻ�Ϊ2 L���ܱ������ڼ���0.2 molA��0.6 molB����һ�������·�����Ӧ��A(s)��3B(g) 2C(s)��3D(g) ��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����±���
2C(s)��3D(g) ��֪�÷�Ӧ�ڲ�ͬ�¶��µ�ƽ�ⳣ�����±���
| �¶�/�� | 1000 | 1150 | 1300 |
| ƽ�ⳣ�� | 64��0 | 50.7 | 42��9 |
�Ÿ÷�Ӧ��ƽ�ⳣ������ʽK�� ����H 0(���������)��
��1000 ��ʱ,4 min��ﵽƽ�⣮��4 min��D��ƽ����Ӧ����v(D)�� ��B��ƽ��ת����Ϊ ��ƽ��ʱB��������� ��
������ߢ���B��ƽ��ת���ʣ��ɲ�ȡ�Ĵ�ʩ��
A������C���� B������A���� C���Ƴ�����D
D�����ͷ�Ӧ�¶� E����С�������ݻ� F��������ʵĴ���
��1000 ��ʱ, ��һ�ݻ�Ϊ2 L���ܱ������ڼ���XmolC��0.6 molD��5 min��ﵽƽ�⣬B��Ũ�������B��Ũ����ͬ����X�ķ�Χ
������˵������˵����Ӧ�Ѵﵽƽ��״̬����
A�������ڻ�������ѹǿ����ʱ��仯���� B��B�����ʲ���ʱ��ı仯���仯
C��c(B)�Uc(D)=1�U1 D�����������ܶȱ��ֲ���(M(B)��M(D))
2013��9�£��й��������е������������ص������������������ӱ������ϵȵصĿ�����Ⱦ��Ϊ6��������Ⱦ�������ض���Ⱦ������β����ȼú����������ȡů�ŷŵ�CO2�ȶ��������γɵ�ԭ��
��1������β����������Ҫԭ��Ϊ;2NO(g)��2CO(g) N2��g)��2CO2��g)�� ��H��0����һ���¶��£���һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬��
N2��g)��2CO2��g)�� ��H��0����һ���¶��£���һ����̶����ܱ������г���һ������NO��CO��t1ʱ�̴ﵽƽ��״̬��
�����жϸ÷�Ӧ�ﵽƽ��״̬�ı�־�ǣߣߣߣߡ�
| A���ڵ�λʱ��������1mol CO2��ͬʱ������lmol CO |
| B�����������ܶȲ��ٸı� |
| C����������ƽ����Է����������ٸı� |
| D����������ѹǿ���ٱ仯 |

����Ҫͬʱ��߸÷�Ӧ�����ʺ�NO��ת���ʣ���ȡ�Ĵ�ʩ��_____��____����д��2����
(2���ı�ú�����÷�ʽ�ɼ��ٻ�����Ⱦ��ͨ���ɽ�ˮ����ͨ�����ȵ�̼�õ�ˮú�����䷴Ӧԭ��ΪC(s)��H2O(g)
 CO(g)��H2(g) ��H��+131.3kJ/mol��
CO(g)��H2(g) ��H��+131.3kJ/mol���ٸ÷�Ӧ��___�����Է����У�����¡����¡�����
��ú���������в������к�����H2S����������Na2C03��Һ���գ��÷�Ӧ�����ӷ���ʽΪ____������֪��H2S�� Ka1��9.1��10-8��Ka2��1.1��10-12��H2CO3��Ka1��4.30��10-7��Ka2��5.61��10-11��
(3����֪��Ӧ��CO(g����H2O��g��
 CO2��g����H2��g�����ֽ���ͬ����CO��g����H2O��g���ֱ�ͨ�˵����Ϊ2L�ĺ����ܱ������н��з�Ӧ���õ������������ݣ�
CO2��g����H2��g�����ֽ���ͬ����CO��g����H2O��g���ֱ�ͨ�˵����Ϊ2L�ĺ����ܱ������н��з�Ӧ���õ������������ݣ�| ʵ�� | �¶�/�� | ��ʼ��/mol | ƽ����/mol | ��ƽ������ʱ��/min | ||
| CO | H2O | H2 | CO | |||
| 1 | 650 | 4 | 2 | 1.6 | 2.4 | 6 |
| 2 | 900 | 2 | 1 | 0.4 | 1.6 | 3 |
| 3 | 900 | a | b | c | d | t |
��ʵ��1������ƽ�ⳣ��K��______������С������λ����
��ʵ��3�У���ƽ��ʱ��CO��ת���ʴ���ˮ��������a��b��������Ĺ�ϵ��______��
�۸÷�Ӧ�ġ�H ______0(�����������������9000Cʱ������һ��ʵ�飬�ڴ������м���l0mol CO,5mo1 H2O,2mo1 CO2,5mol H2�����ʱ����______�������������������������������
�״�����Ҫ�Ļ�ѧ��ҵ����ԭ�Ϻ�Һ��ȼ�ϡ���ҵ�Ͽ�����CO��CO2������ȼ�ϼ״�����֪�״��Ʊ����йػ�ѧ��Ӧ�Լ��ڲ�ͬ�¶��µĻ�ѧ��Ӧƽ�ⳣ�����±���ʾ��
| ��ѧ��Ӧ | ƽ�ⳣ�� | �¶ȣ��棩 | |
| 500 | 800 | ||
��2H2(g)+CO(g)  CH3OH(g) CH3OH(g) | K1 | 2��5 | 0��15 |
��H2(g)+CO2(g)  H2O (g)+CO(g) H2O (g)+CO(g) | K2 | 1��0 | 2��50 |
��3H2(g)+ CO2(g)  CH3OH(g)+H2O (g) CH3OH(g)+H2O (g) | K3 | | |
��1����Ӧ���� ������ȡ����ȡ�����Ӧ��
��2��ij�¶��·�Ӧ����H2��ƽ��ת���ʣ�a������ϵ��ѹǿ(P)�Ĺ�ϵ��ͼ��ʾ����ƽ��״̬��A�䵽Bʱ��ƽ�ⳣ��K(A) K(B)�����������������������
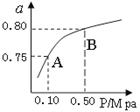
��3���жϷ�Ӧ�ۡ�H 0�� ��S 0���>����=����<�����ݷ�Ӧ����ڿ��Ƶ���K1��K2��K3֮��Ĺ�ϵ����K3= ����K1��K2��ʾ������500�桢2L���ܱ������У����з�Ӧ�ۣ����ijʱ��H2��CO2�� CH3OH��H2O�����ʵ����ֱ�Ϊ6mol��2 mol��10 mol��10 mol����ʱv(��) v(��)���>����=����<����
��4��һ���¶��£���3 L�ݻ��ɱ���ܱ������з�����Ӧ�ڣ���֪c(CO)�뷴Ӧʱ��t�仯���ߢ���ͼ��ʾ������t0ʱ�̷ֱ�ı�һ�����������ߢ��Ϊ���ߢ�����ߢ�
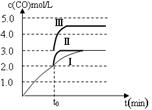
�����ߢ��Ϊ���ߢ�ʱ���ı�������� ��
�����ߢ��Ϊ���ߢ�ʱ���ı�������� ��
��5���״�ȼ�ϵ��ͨ�����ò��缫���乤��ԭ����ͼ��ʾ�������ĵ缫��ӦΪ�� ��
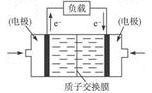
��6��һ�������¼״���һ����̼��Ӧ���Ժϳ����ᡣͨ��״���£���0��2 mol/L�Ĵ�����0��1 mol/LBa(OH)2��Һ�������ϣ�������Һ������Ũ���ɴ�С��˳��Ϊ ��
 B(g) +C(g)���ݻ�Ϊ1.0L���ܱ������н��У�A�ij�ʼŨ��Ϊ0.050mol/L���¶�T1��T2��A��Ũ����ʱ���ϵ��ͼ��ʾ���ش��������⣺
B(g) +C(g)���ݻ�Ϊ1.0L���ܱ������н��У�A�ij�ʼŨ��Ϊ0.050mol/L���¶�T1��T2��A��Ũ����ʱ���ϵ��ͼ��ʾ���ش��������⣺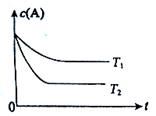
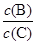 �� (���������С�����䡱)��
�� (���������С�����䡱)��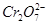 ��
��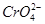 �����õķ��������֡�
�����õķ��������֡�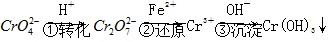 ��
��
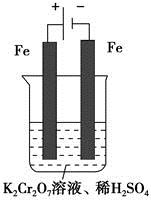
 B(g)��C(g)�������ֲ�ͬ�����½��У�����ʵ�����800��C��ʵ�����850��C��B��C����ʼŨ�ȶ�Ϊ0����Ӧ��A��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ��
B(g)��C(g)�������ֲ�ͬ�����½��У�����ʵ�����800��C��ʵ�����850��C��B��C����ʼŨ�ȶ�Ϊ0����Ӧ��A��Ũ��(mol��L��1)��ʱ��(min)�ı仯��ͼ��ʾ��