题目内容
9.下列反应的化学方程式或离子方程式书写正确的是( )| A. | 氯乙烷中加入硝酸银溶液:Cl-+Ag+═AgCl↓ | |
| B. | 溴乙烷与氢氧化钠水溶液共热:CH3CH2Br+NaOH$→_{△}^{H_{2}O}$CH2═CH2↑+NaBr+H2O | |
| C. | 丙烯聚合:nCH2═CHCH3$→_{△}^{催化剂}$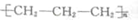 | |
| D. | 苯酚钠溶液中通入少量二氧化碳: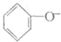 +CO2+H2O→ +CO2+H2O→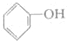 +HCO3- +HCO3- |
分析 A.氯乙烷为非电解质,不能电离出氯离子;
B.溴乙烷与氢氧化钠水溶液共热,发生水解反应;
C.聚合物结构简式错误;
D.苯酚钠溶液中通入少量二氧化碳生成苯酚和碳酸氢钠.
解答 解:A.氯乙烷为非电解质,与硝酸银溶液不反应,故A错误;
B.溴乙烷与氢氧化钠水溶液共热,发生水解反应生成乙醇,应为CH3CH2Br+NaOH$→_{△}^{H_{2}O}$CH3CH2OH+NaBr,故B错误;
C.聚合物结构简式错误,应为 ,故C错误;
,故C错误;
D.苯酚钠溶液中通入少量二氧化碳生成苯酚和碳酸氢钠,离子方程式为 +CO2+H2O→
+CO2+H2O→ +HCO3-,故D正确.
+HCO3-,故D正确.
故选D.
点评 本题考查离子反应及化学反应方程式书写的正误判断,为高频考点,把握发生的反应为解答的关键,注意常见有机物的性质及反应,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列有关说法正确的是( )
| A. | 常温下,向醋酸溶液中加入少量的水,溶液中c(H+)将增大 | |
| B. | 常温下,pH相同的NaOH溶液和Ba(OH)2溶液中,水的电离程度相同 | |
| C. | 向NaHCO3溶液中加入少量的澄清石灰水,所得溶液的pH不变 | |
| D. | 常温下,2NO(g)+2CO(g)═N2(g)+2CO(g)能自发进行,则该反应的△H>0 |
17.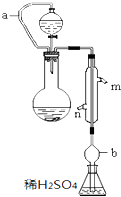 实验小组测定某肥料中的总氮含量(以氮的质量分数表示),实验装置如图(图中加热及夹持仪器略去).称取1.200g样品,通过化学方法将肥料中的氮转化成铵盐(除样品外,所加试剂均不含氮元素),然后在碱性溶液中蒸馏氨,用25.00mL浓度为0.5000mol•L-1硫酸溶液充分吸收,再用浓度为0.1000mol•L-1氢氧化钠溶液滴定未反应的硫酸.重复上述实验三次.实验数据如下:
实验小组测定某肥料中的总氮含量(以氮的质量分数表示),实验装置如图(图中加热及夹持仪器略去).称取1.200g样品,通过化学方法将肥料中的氮转化成铵盐(除样品外,所加试剂均不含氮元素),然后在碱性溶液中蒸馏氨,用25.00mL浓度为0.5000mol•L-1硫酸溶液充分吸收,再用浓度为0.1000mol•L-1氢氧化钠溶液滴定未反应的硫酸.重复上述实验三次.实验数据如下:
(1)写出圆底烧瓶内发生反应的离子方程式NH4++OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O.
(2)分液漏斗和圆底烧瓶之间的导管a的作用是保证烧瓶和漏斗内压强恒定,有利于漏斗中的液体滴入锥形瓶中,b的作用是防止锥形瓶中的溶液倒吸.
(3)在滴定过程中,以下操作会使所测总氮含量偏小的是(填序号)BD.
A.锥形瓶水洗后未烘干 B.滴定过程中滴定管有漏水现象
C.滴定过程中有少量溶液从锥形瓶中溅出 D.滴定前滴定管内有气泡,滴定后没有了
(4)若实验操作均正确,但测定结果偏低,可能造成该结果的主要原因是仍有氨气残留在装置中未被锥形瓶中的硫酸吸收.
(5)利用题目中所给数据计算肥料中总氮含量为28.6%(计算结果保留到小数点后1位).
 实验小组测定某肥料中的总氮含量(以氮的质量分数表示),实验装置如图(图中加热及夹持仪器略去).称取1.200g样品,通过化学方法将肥料中的氮转化成铵盐(除样品外,所加试剂均不含氮元素),然后在碱性溶液中蒸馏氨,用25.00mL浓度为0.5000mol•L-1硫酸溶液充分吸收,再用浓度为0.1000mol•L-1氢氧化钠溶液滴定未反应的硫酸.重复上述实验三次.实验数据如下:
实验小组测定某肥料中的总氮含量(以氮的质量分数表示),实验装置如图(图中加热及夹持仪器略去).称取1.200g样品,通过化学方法将肥料中的氮转化成铵盐(除样品外,所加试剂均不含氮元素),然后在碱性溶液中蒸馏氨,用25.00mL浓度为0.5000mol•L-1硫酸溶液充分吸收,再用浓度为0.1000mol•L-1氢氧化钠溶液滴定未反应的硫酸.重复上述实验三次.实验数据如下:| 实验 次数 | 氢氧化钠溶液的体积 | |
| 滴定前刻度(mL) | 滴定后刻度(mL) | |
| 1 | 0.00 | 5.22 |
| 2 | 6.00 | 11.18 |
| 3 | 12.00 | 17.20 |
(2)分液漏斗和圆底烧瓶之间的导管a的作用是保证烧瓶和漏斗内压强恒定,有利于漏斗中的液体滴入锥形瓶中,b的作用是防止锥形瓶中的溶液倒吸.
(3)在滴定过程中,以下操作会使所测总氮含量偏小的是(填序号)BD.
A.锥形瓶水洗后未烘干 B.滴定过程中滴定管有漏水现象
C.滴定过程中有少量溶液从锥形瓶中溅出 D.滴定前滴定管内有气泡,滴定后没有了
(4)若实验操作均正确,但测定结果偏低,可能造成该结果的主要原因是仍有氨气残留在装置中未被锥形瓶中的硫酸吸收.
(5)利用题目中所给数据计算肥料中总氮含量为28.6%(计算结果保留到小数点后1位).
19.下列化学用语书写正确的是( )
| A. | 氯原子的结构示意图: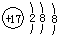 | B. | CH4分子的球棍模型: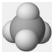 | ||
| C. | 氯化镁的电子式: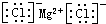 | D. | N2的结构式: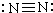 |
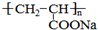 )是一种强吸水树脂.由某烃A合成聚丙烯酸钠的流程如图:
)是一种强吸水树脂.由某烃A合成聚丙烯酸钠的流程如图: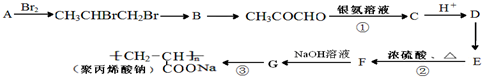
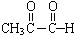 +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$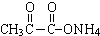 +3NH3+2Ag↓+H2O.
+3NH3+2Ag↓+H2O.
 .
.