题目内容
下列各组热化学方程式的ΔH前者大于后者的是
①C(s)+O2(g)===CO2(g) ΔH1
C(s)+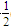 O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2
②S(s)+O2(g)===SO2(g) ΔH3
S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+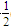 O2(g)===H2O(l) ΔH5
O2(g)===H2O(l) ΔH5
2H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7
CaO(s)+H2O(l)==="Ca" (OH)2(s) ΔH8
①C(s)+O2(g)===CO2(g) ΔH1
C(s)+
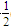 O2(g)===CO(g) ΔH2
O2(g)===CO(g) ΔH2②S(s)+O2(g)===SO2(g) ΔH3
S(g)+O2(g)===SO2(g) ΔH4
③H2(g)+
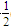 O2(g)===H2O(l) ΔH5
O2(g)===H2O(l) ΔH52H2(g)+O2(g)===2H2O(l) ΔH6
④CaCO3(s)===CaO(s)+CO2(g) ΔH7
CaO(s)+H2O(l)==="Ca" (OH)2(s) ΔH8
| A.① | B.④ | C.②③④ | D.①②③ |
C
试题分析:①碳的燃烧反应是放热反应,ΔH<0;等质量的碳完全燃烧生成二氧化碳时放出的热量比不完全燃烧生成一氧化碳时放出的热量多,放热越多,ΔH越小,ΔH1<ΔH2。②等质量的气态硫单质完全燃烧生成二氧化硫时放出的热量比固态硫单质完全燃烧生成二氧化硫时放出的热量多,放出的热量越多,ΔH越小,ΔH4<ΔH3。③都生成液态水的前提下,氢气的质量越大,放出的热量越多,ΔH越小,ΔH6<ΔH5。④碳酸钙受热分解是吸热反应,ΔH>0;氧化钙溶于水是放热反应,ΔH<0, ΔH8<ΔH7。
点评:此类题只要知道化学反应热效应的类型和判断其大小的方法,较为简单

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
 C(g) +D(g)过程中的能量变化如右图所示,则该反应是__________________反应 (填“吸热”或“放热”)。若使用催化剂,反应的△H (填“增大”或“减小”或“不变”)。
C(g) +D(g)过程中的能量变化如右图所示,则该反应是__________________反应 (填“吸热”或“放热”)。若使用催化剂,反应的△H (填“增大”或“减小”或“不变”)。 
 =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·
 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ· =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·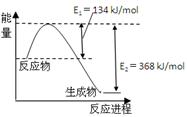
 N2(g)+2CO2(g)的△H是 。
N2(g)+2CO2(g)的△H是 。