��Ŀ����
����Ŀ����ɫ��������(KO2)����Ϊ����ɴ��յ���Դ��ijѧϰС���������ʵ��̽��KO2�����ʣ���ش�������⣺
I.̽��KO2��ˮ�ķ�Ӧ��ȡ����KO2�������Թ��У��μ�����ˮ���ٲ������ݣ��������ǵ�ľ�������Թܿ�ľ����ȼ���μӷ�̪��Һ���ȱ�����ɫ��
����ɫ����Һ�еμ�FeCl3��Һ�Ʋ����������Ϊ___��
II.̽��KO2��SO2�ķ�Ӧ
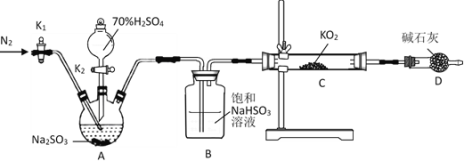
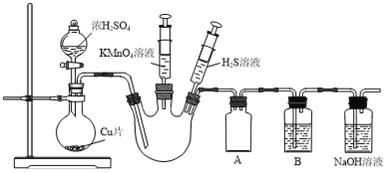
��1����ȷ�IJ���������__��
�ٴ�K1ͨ��N2 ���ž�װ����ԭ�����ر� �ڲ�жװ����ʵ�����
�ۼ��װ�������ԣ�Ȼ��װ��ҩƷ �ܴ�Һ©������K2
��2���������װ�������Եķ�����___��
��3��Aװ�÷����Ļ�ѧ����ʽΪ___��
��4��������װ����֤��KO2��SO2��Ӧ����O2�������ڲ��㣬��ĸĽ���ʩ��__��
��5���Ľ�����ʵ�飬��KO2��ȫ��Ӧ��װ��C�й����ˮ�ܽ⣬���50.00mL��Һ���ȷ�ΪM��N���ݡ�
����M��Һ�м��������������ữ��BaCl2��Һ����ַ�Ӧ���������ˡ�__��__������Ϊ2.33g��
�ڽ�N��Һ����__�����������ƣ��У���0.40mol/L����KMnO4��Һ�ζ����յ�ʱ��������KMnO4��Һ20.00mL��
������������������ݣ���д����ʵ���ܷ�Ӧ�Ļ�ѧ����ʽ__��
���𰸡��������ɫ���������� �ۢ٢ܢ٢ڻ�ۢܢ٢� װ��ĩ������һ���ܲ���ˮ�У���A��ĩ�������ݣ���ȴ�����һ��ˮ�����ֲ��� H2SO4+Na2SO3��Na2SO4+H2O+SO2�� ��B��C֮������һ��ʢ��Ũ�����ϴ��ƿ�����߽�Bװ���еı���NaHSO3��Һ�滻ΪŨ���ᣩ ϴ�� ���� ��ƿ 6KO2+3SO2��2K2SO3+K2SO4+4O2
��������
Aװ����70%��H2SO4���������Ʒ�Ӧ���ɶ������ݴ���д��Ӧ�Ļ�ѧ����ʽ����ʵ���װ��ͼ��֪������Ӳ�ʲ����ܵ������к���ˮ������2.33g����Ϊ���ᱵ������������������Ʒ�Ӧ�ķ���ʽΪ2KMnO4+5K2SO3+3H2SO4=6K2SO4+2MnSO4+3H2O����������ɵ�����غ�������ص����ʵ���֮�ȣ�Ȼ����д��Ӧ�ķ���ʽ�����ݴ˷������н��
KO2�����еμ�����ˮ����Ӧ����Һ�еμ�FeCl3��Һ���Ȼ������������ط�Ӧ���������������ɫ������ͬʱ�Ȼ�������������ֽ�ų���������˿���������Ϊ�������ɫ���������塣
��1��������ʾ��ʵ����������ʵ��װ��ͼ��ʵ�鲽��Ϊ�����ȼ��װ�������ԣ�Ȼ��װ��ҩƷ����K1ͨ��N2���ž�װ���ڵĿ�����رգ��ٴ�Һ©������K2����Ӧ���ɶ�������K1ͨ��N2���ž�װ���ڵĶ��������رգ���жװ����ʵ����ɡ��ʴ�Ϊ�ۢ٢ܢ٢ڻ�ۢܢ٢ڡ�
��2����װ��ĩ������һ���ܲ���ˮ�У�������A�����ĩ�������ݲ���������ȴ�����һ��ˮ�����ֲ��䣬��װ�����������á�
��3��Aװ����70%��H2SO4���������Ʒ�Ӧ�ų������������壬��Ӧ�Ļ�ѧ����ʽΪH2SO4 + Na2SO3��Na2SO4 + H2O + SO2����
��4����ʵ���װ��ͼ��֪������Ӳ�ʲ����ܵ������к���ˮ������������ʵ����֤��KO2��SO2��Ӧ����O2�������Ľ���ʩΪ��B��C֮������һ��ʢ��Ũ�����ϴ��ƿ(���߽�Bװ���еı���NaHSO3��Һ�滻ΪŨ����)��
��5������M��Һ�м��������������ữ��BaCl2��Һ����ַ�Ӧ���������ˡ�ϴ�ӡ�����֮����ء�
�ڽ�N��Һ������ƿ�н��еζ�������
��2.33g����Ϊ���ᱵ�����ʵ���=![]() =0.01mol�����ԭ��Ʒ�к���0.02mol����أ�����������������Ʒ�Ӧ�ķ���ʽΪ2KMnO4+5K2SO3+3H2SO4=6K2SO4+2MnSO4+3H2O�����ԭ��Ʒ��������ص����ʵ���=2��
=0.01mol�����ԭ��Ʒ�к���0.02mol����أ�����������������Ʒ�Ӧ�ķ���ʽΪ2KMnO4+5K2SO3+3H2SO4=6K2SO4+2MnSO4+3H2O�����ԭ��Ʒ��������ص����ʵ���=2��![]() ��0.40mol/L��0.020L=0.04mol�����KO2��SO2��Ӧ�Ļ�ѧ����ʽΪ6KO2+3SO2��2K2SO3+K2SO4+4O2��
��0.40mol/L��0.020L=0.04mol�����KO2��SO2��Ӧ�Ļ�ѧ����ʽΪ6KO2+3SO2��2K2SO3+K2SO4+4O2��

 ȫ�ų��100��ϵ�д�
ȫ�ų��100��ϵ�д� Ӣ�ŵ��ϵ�д�
Ӣ�ŵ��ϵ�д�����Ŀ��������25 ��ʱ�������ܵ���ʵ��ܽ�ȣ�
���ܵ���� | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
�ܽ��/g | 9��10-4 | 1.7��10-6 | 1.5��10-4 | 3.0��10-9 |
������������ᴿ�У����������ܵ���ʵ��ܽ�ƽ��ԭ����ȥijЩ�������ӡ����磺
��Ϊ��ȥ�Ȼ���е�����Fe3+���Ƚ����������ˮ���ټ���һ�������Լ���Ӧ�����˽ᾧ���ɣ�
��Ϊ��ȥ�Ȼ�þ�����е�����Fe3+���Ƚ����������ˮ������������������þ����ַ�Ӧ�����˽ᾧ���ɣ�
��Ϊ��ȥ����ͭ�����е�����Fe2+���Ƚ����������ˮ������һ������H2O2����Fe2+������Fe3+��������Һ��pH=a�����˽ᾧ���ɡ�
��ش��������⣺
��1���������ֳ��ӷ������ܹ��ﵽ�ܺõ�Ч����Fe3+��Fe2+����ת��Ϊ__________________(�ѧʽ)����ȥ��
��2�����м�����Լ�Ӧ��ѡ��__________Ϊ�ˣ���ԭ����______________________________��
��3�����г�ȥFe3+���������ܷ�Ӧ�����ӷ���ʽΪ____________________________________��
��4����֪Fe(OH)3��Ksp=1��10-35 ����ѧ��ͨ����Ϊ��������Һ������Ũ��С����1��10-5mol/Lʱ��������ȫ����������a��СֵΪ________________��
��5�������뷽������ص������У���ȷ����___________________________(����ĸ)��
A��H2O2����ɫ�������������������в��������ʣ���������Ⱦ
B����Fe2+����ΪFe3+����Ҫԭ����Fe(OH)2������Fe(OH)3�������ѹ���
C��������ҺpH=a��ѡ����Լ���������ͭ���ʽ̼��ͭ
D��Cu2+���Դ���������pH=a����Һ��
E����pH>a����Һ��Fe3+һ�����ܴ�������
����Ŀ���¶ȷֱ�ΪT1��T2ʱ��������X������Y��0.16mol����10L�����ܱ������У�������ӦX(g)+Y(g)![]() 2Z(g)��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±���
2Z(g)��һ��ʱ���ﵽƽ�⣬��Ӧ�����вⶨ���������±���
�¶�/K | t/min | t1 | t2 | t3 | t4 |
T1 | n(Y)/mol | 0.14 | 0.12 | 0.10 | 0.10 |
T2 | n(Y)/mol | 0.13 | 0.09 | 0.08 |
����˵����ȷ���ǣ� ��
A. �÷�Ӧ������ӦΪ���ȷ�Ӧ
B. T2�¶��´˷�Ӧ��ƽ�ⳣ��K=4
C. �¶�ΪT1ʱ��0~t1ʱ��ε�ƽ��������(Z)=2.0��10��3mol��L��1��min��1
D. ��T1��ƽ����������������䣬�ٳ���0.2molZ��ƽ��ʱX�������������