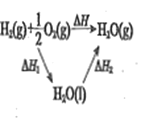题目内容
【题目】按要求填空:
(1)单质铝和氢氧化钾溶液反应的化学方程式:_____________________________。
(2)单质镁与二氧化碳反应的化学方程式:______________________________。
(3)工业制备粗硅的化学方程式:_________________________________________。
(4)氨的催化氧化反应:____________________________________________。
(5)实验室制氯气的离子方程式:__________________________________________。
(6)硫代硫酸钠与盐酸反应的离子方程式:_____________________________。
【答案】2Al + 2KOH +2H2O=2KAlO2 + 3H2↑ 2Mg+CO2 ![]() 2MgO+C SiO2+2C
2MgO+C SiO2+2C![]() Si+2CO↑ 4NH3+5O2
Si+2CO↑ 4NH3+5O2![]() 4NO+6H2O MnO2+2Cl-+4H+
4NO+6H2O MnO2+2Cl-+4H+![]() Cl2↑+Mn2++2H2O S2O32-+2H+=SO2↑+S↓+H2O
Cl2↑+Mn2++2H2O S2O32-+2H+=SO2↑+S↓+H2O
【解析】
(1)铝和氢氧化钾溶液反应生成偏铝酸钾和氢气;(2)镁在二氧化碳中燃烧反应生成碳与氧化镁;(3)工业上用SiO2与碳在高温下制备粗硅;(4)NH3与O2在催化剂、加热条件下发生反应生成一氧化氮和水;(5)实验室中用二氧化锰和浓盐酸反应来制取氯气;(6)硫代硫酸钠在酸性条件下发生歧化反应,生成二氧化硫、S、水;据此书写方程式。
(1)铝和氢氧化钾溶液反应生成偏铝酸钾和氢气,反应的化学方程式:2Al + 2KOH +2H2O=2KAlO2 + 3H2↑,故答案为:2Al + 2KOH +2H2O=2KAlO2 + 3H2↑;
(2)镁在二氧化碳中燃烧反应生成碳与氧化镁,反应的化学方程式为2Mg+CO2 ![]() 2MgO+C,故答案为:2Mg+CO2
2MgO+C,故答案为:2Mg+CO2 ![]() 2MgO+C;
2MgO+C;
(3)工业上用石英(主要成分为SiO2)制备粗硅,反应的化学方程式为:SiO2+2C![]() Si+2CO↑,故答案为:SiO2+2C
Si+2CO↑,故答案为:SiO2+2C![]() Si+2CO↑;
Si+2CO↑;
(4)氨气具有还原性,氧气具有氧化性,氨气和氧气反应生成一氧化氮和水,反应方程为:4NH3+5O2![]() 4NO+6H2O,故答案为:4NH3+5O2
4NO+6H2O,故答案为:4NH3+5O2![]() 4NO+6H2O;
4NO+6H2O;
(5)实验室中用二氧化锰和浓盐酸反应来制取氯气,离子方程式为:MnO2+2Cl-+4H+![]() Cl2↑+Mn2++2H2O,故答案为:MnO2+2Cl-+4H+
Cl2↑+Mn2++2H2O,故答案为:MnO2+2Cl-+4H+![]() Cl2↑+Mn2++2H2O;
Cl2↑+Mn2++2H2O;
(6)硫代硫酸钠与盐酸发生氧化还原反应生成二氧化硫、S、水,离子反应为S2O32-+2H+=SO2↑+S↓+H2O,故答案为:S2O32-+2H+=SO2↑+S↓+H2O。

【题目】下列实验结果不能作为相应定律或原理的证据之一的是( )
(阿伏加德罗定律:在同温同压下,相同体积的任何气体含有相同数目的分子)
A | B | C | D | |
勒夏特列原理 | 元素周期律 | 盖斯定律 | 阿伏伽德罗定律 | |
实验方案 |
|
|
|
|
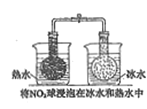
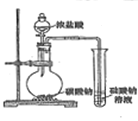
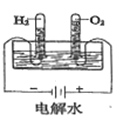
结果 | 左球气体颜色加深 右球气体颜色变浅 | 烧瓶中冒气泡 试管中出现浑浊 | 测得 |
|
A. AB. BC. CD. D
【题目】用某铜矿(含CuS以及少量FeO和Fe2O3)制备CuCl的主要流程如下:
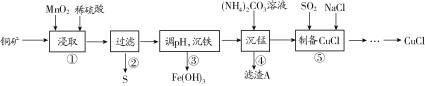
已知Fe3+、Mn2+、Cu2+生成氢氧化物沉淀时的pH如下表所示:
物质 | 开始沉淀 | 沉淀完全 |
Fe(OH)3 | 2.7 | 3.7 |
Mn(OH)2 | 7.1 | 10.1 |
Cu(OH)2 | 4.7 | 6.7 |
(1)浸取时,CuS被浸取的离子方程式为CuS+MnO2+4H+=Cu2++Mn2++S↓+2H2O,该反应的氧化剂是________(填化学式),Fe2O3被浸取的离子方程式为________________。
(2)步骤③调整pH的范围为______,滤渣A的成分为________(填化学式)。
(3)“沉铁”时,需要检验Fe3+是否沉淀完全,所用的试剂为________(填化学式)。
(4)准确称取所制备的氯化亚铜样品1.600 g,将其置于足量的FeCl3溶液中,待样品完全溶解后,加入适量稀硫酸,用0.100 0 mol·L-1的K2Cr2O7溶液滴定到终点,消耗K2Cr2O7溶液25.00 mL,反应中Cr2O72-被还原为Cr3+,计算样品中CuCl的质量分数(写出计算过程)______。
【题目】利用如图所示装置进行下列实验,能得出相应实验结论的是( )

选项 | ① | ② | ③ | 实验结论 |
A | 浓盐酸 | KMnO4 | 紫色石蕊试液 | 氯气具有酸性、漂白性 |
B | 浓硫酸 | 蔗糖 | 溴水 | 浓硫酸具有脱水性、氧化性 |
C | 稀硝酸 | Na2SO3 | 品红溶液 | 实验室制取并检验SO2 |
D | 浓硝酸 | Na2CO3 | Na2SiO3溶液 | 非金属性:N>C>Si |
A.AB.BC.CD.D