题目内容
7.下列实验操作和对应的现象、结论都正确的是( )| 选项 | 操作 | 现象 | 结论 |
| A | 将足量的乙烯通入到溴水中 | 溴水褪色 | 乙烯与溴水反应生成无色物质 |
| B | 往CaCl2溶液中通入足量的CO2 | 先有白色沉淀生成,后沉淀溶解 | CaCO3不溶于水,Ca(HCO3)2可溶于水 |
| C | 将铜板电路投入FeCl3溶液中 | 铜溶于FeCl3溶液 | 氧化性:Fe3+>Cu2+ |
| D | 取久置的Na2O2粉末,向其中滴加足量的盐酸 | 产生无色气体 | Na2O2已变质为Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.乙烯中含有碳碳双键,性质较活泼,能和溴发生加成反应;
B.碳酸酸性小于盐酸,弱酸不能和强酸盐反应生成强酸;
C.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性;
D.Na2O2、Na2CO3都能和稀盐酸反应生成无色气体.
解答 解:A.乙烯中含有碳碳双键,性质较活泼,能和溴发生加成反应生成无色物质1,2-二溴乙烷,所以溴水褪色,故A正确;
B.碳酸酸性小于盐酸,弱酸不能和强酸盐反应生成强酸,碳酸酸性小于盐酸,所以二氧化碳和氯化钙溶液不反应,则没有沉淀生成,故B错误;
C.同一氧化还原反应中,氧化剂的氧化性大于氧化产物的氧化性,发生的反应为2Fe3++Cu=Cu2++2Fe2+,该反应中氧化剂是Fe3+、氧化产物是Cu2+,所以氧化性:Fe3+>Cu2+,故C正确;
D.Na2O2、Na2CO3都能和稀盐酸反应生成无色气体,所以不能根据产生无色气体判断是否变质,故D错误;
故选AC.
点评 本题考查化学实验方案评价,为高频考点,涉及物质检验、氧化性强弱比较、酸性强弱比较等知识点,明确实验原理是解本题关键,熟练掌握元素化合物知识,易错选项是B.

练习册系列答案
 53随堂测系列答案
53随堂测系列答案
相关题目
19.下列实验操作不能达到实验目的是( )
| A. | 用酸性高锰酸钾溶液鉴别乙烷与乙烯 | |
| B. | 向蔗糖溶液中加入稀硫酸,加热,冷却后加入新制Cu(OH)2检验水解产物 | |
| C. | 用饱和Na2CO3溶液鉴别乙酸、乙醇、硝基苯 | |
| D. | 利用燃烧的方法鉴别羊毛和棉花 |
14. 键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.参考以下表格的键能数据,回答下列问题:
键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.参考以下表格的键能数据,回答下列问题:
(1)比较下列两组物质的熔点高低(填“>”或“<”)
SiC>Si; SiCl4<SiO2
(2)能不能根据键能的数据判断单质Si 和化合物SiCl4的熔点高低?不能(填“能”或“不能”),理由是物质熔点高低由构成物质的微粒间作用力决定,单质Si属于原子晶体,原子间作用力是共价键;SiCl4属于分子晶体,分子间作用力是范德华力,比共价键弱得多.因此不能都根据键能来判断物质的熔点高低(提示对比二者晶体类型及内部微粒作用力)
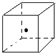
(3)如图立方体中心的“•”表示金刚石晶体中的一个原子,请在立方体的顶点用“•”表示出与之紧邻的碳原子;
(4)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g)
计算该反应的反应热△H为+236 kJ/mol(要包含数据和焓变单位)
 键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.参考以下表格的键能数据,回答下列问题:
键能的大小可以衡量化学键的强弱,也可以用于估算化学反应的反应热(△H),化学反应的△H等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差.参考以下表格的键能数据,回答下列问题:| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
SiC>Si; SiCl4<SiO2
(2)能不能根据键能的数据判断单质Si 和化合物SiCl4的熔点高低?不能(填“能”或“不能”),理由是物质熔点高低由构成物质的微粒间作用力决定,单质Si属于原子晶体,原子间作用力是共价键;SiCl4属于分子晶体,分子间作用力是范德华力,比共价键弱得多.因此不能都根据键能来判断物质的熔点高低(提示对比二者晶体类型及内部微粒作用力)
(3)如图立方体中心的“•”表示金刚石晶体中的一个原子,请在立方体的顶点用“•”表示出与之紧邻的碳原子;
(4)工业上高纯硅可通过下列反应制取:SiCl4(g)+2H2(g)$\frac{\underline{\;高温\;}}{\;}$Si(s)+4HCl(g)
计算该反应的反应热△H为+236 kJ/mol(要包含数据和焓变单位)
 2AB2(g)△H<0,下列说法正确的是( )
2AB2(g)△H<0,下列说法正确的是( ) 2NH3(g) ΔH=-92.4 kJ·m
2NH3(g) ΔH=-92.4 kJ·m ol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是
ol-1,在反应过程中,正反应速率的变化如图:下列说法正确的是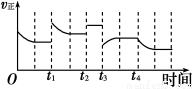

 ,
,

 ⑧
⑧ .
.