题目内容
9.血液中的钙离子平衡在临床医学中具有重要的意义.某研究小组为测定血液样品中Ca2+的含量,进行的实验如下:①量取5.0mL血液样品,处理后配制成100mL溶液;
②量取10.0mL,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀;
③过滤并洗净所得CaC2O4沉淀,用过量稀硫酸溶解,生成H2C2O4和CaSO4稀溶液;
④加入0.001mol•L-1的KMnO4溶液,使H2C2O4完全被氧化,同时产生使澄清石灰水变浑浊的无色无味气体,消耗酸性KMnO4溶液的体积为2.00mL.
(1)步骤①中用到的玻璃仪器有玻璃棒、烧杯、量筒玻璃棒、100ml容量瓶、胶头滴管.
(2)步骤②中发生反应的离子方程式为Ca2++C2O42-=CaC2O4↓.
(3)步骤④中发生的离子方程式为:2MnO4-+5H2C2O4+6H+═2Mn2++8H2O+10CO2↑;氧化产物与还原产物的物质的量之比为5:1.
(4)计算血样中Ca2+的含量(写出计算过程).4×10-4g/ml.
分析 (1)量取5.0mL血液样品,处理后配制成100mL溶液,用到的玻璃仪器依据配制溶液的过程选择所需仪器;
(2)取10.0mL,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀,是钙离子和草酸根离子结合生成;
(3)草酸具有还原性能被酸性高锰酸钾溶液氧化使H2C2O4完全被氧化,生成二氧化碳,2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O,元素化合价升高被氧化得到氧化产物,元素化合价降低被还原得到还原产物,氧化还原反应存在电子守恒据此计算;
(4)根据2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O求出n(CaC2O4)=n(H2C2O4)=n(Ca2+),带入m=nM计算质量得到含量;
解答 解:(1)量取5.0mL血液样品,处理后配制成100mL溶液,用到的玻璃仪器依据配制溶液的过程选择所需仪器,量取需要量筒,溶解需要烧杯和玻璃棒,转移需要100ml容量瓶,定容需要胶头滴管滴定到刻度,需要的玻璃仪器为:玻璃棒、烧杯、量筒、玻璃棒、100ml容量瓶、胶头滴管,
故答案为:玻璃棒、100ml容量瓶、胶头滴管;
(2)取10.0mL,加入过量(NH4)2C2O4溶液,使Ca2+完全转化成CaC2O4沉淀,是钙离子和草酸根离子结合生成,反应的离子方程式为:Ca2++C2O42-=CaC2O4↓,
故答案为:Ca2++C2O42-=CaC2O4↓;
(3)草酸具有还原性能被酸性高锰酸钾溶液氧化使H2C2O4完全被氧化,生成二氧化碳,依据原子守恒和电荷守恒配平得到离子方程式为:2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O,碳元素化合价升高被氧化得到氧化产物为二氧化碳,锰元素化合价降低被还原得到还原产物为Mn2+,氧化还原反应存在电子守恒计算氧化产物与还原产物的物质的量之比为10:2=5:1,
故答案为:10CO2↑,5:1;
(4)根据反应的离子方程式2MnO4-+5H2C2O4+6H+═10CO2↑+2Mn2++8H2O
2 5
0.0010mol/L×0.002L n(H2C2O4)
求出n(CaC2O4)=n(H2C2O4)=n(Ca2+)=5×10-6mol,
5.0mL血液中含钙离子物质的量5×10-6mol×$\frac{100ml}{10ml}$=5×10-5mol
血样中Ca2+的含量=$\frac{5×1{0}^{-5}mol×40g/mol}{5ml}$=4×10-4g/ml,
故答案为:4×10-4g/ml.
点评 本题考查了溶液配制的实验过程分析判断,滴定实验的理解应用、离子反应方程式的书写以及计算,综合性较强,正确书写离子反应方程式是计算的关键,题目难度中等.

| A. | 1 mol Mg 原子变成 Mg2+时失去的电子数为2 NA | |
| B. | 标准状况下,11.2 L H2O所含的电子数为5 NA | |
| C. | 常温常压下,16g O2 与16gO3含有的原子数为相同 | |
| D. | 0.1 mol/L K2SO4 溶液中含有 K+为0.2 NA |


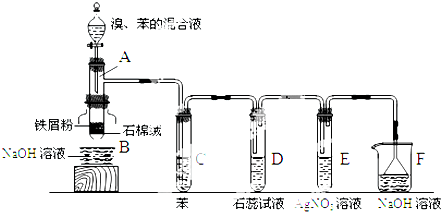
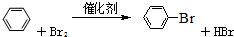 .
.