题目内容
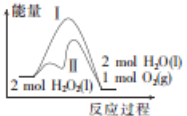
【题目】反应2H2O2(l)![]() 2H2O(l)+O2(g)能量变化如图所示,下列说法错误的是
2H2O(l)+O2(g)能量变化如图所示,下列说法错误的是
A.该反应放热
B.反应速率:途径Ⅱ>途径Ⅰ
C.1 mol H2O2(l)的能量高于1 mol H2O(l)的能量
D.途径Ⅰ放出的热量多
【答案】D
【解析】
A. 反应物能量比生成物的高,所以该反应是放热反应,A正确;
B. 途径II反应比途径I反应所需活化能低,更多物质分子变为活化分子,物质反应放出热量,使物质内能增加,反应速率加快,所以反应速率:途径Ⅱ>途径Ⅰ,B正确;
C. 根据图示2 molH2O2具有的能量比2 molH2O和1 mol O2的能量高,O2也具有能量,故1 mol H2O2(l)的能量高于1 mol H2O(l)的能量,C正确;
D. 反应放出热量与反应途径无关,只与反应物、生成物的总能量有关,故两种途径放出热量相等,D错误;
故合理选项是D。

【题目】以下是处于研究阶段的“人工固氮”的新方法.N2在催化剂表面与水发生反应:
2N2(g)+6H2O(l)4NH3(g)+3O2(g) △H="+" 1530.4kJ/mol;完成下列填空:
(1)该反应平衡常数K的表达式_______.
(2)上述反应达到平衡后,保持其他条件不变,升高温度,重新达到平衡,则______.
a.平衡常数K增大
b.H2O的浓度减小
c.容器内的压强增大
d.v逆(O2)减小
(3)研究小组分别在四个容积为2升的密闭容器中,充入N21mol、H2O 3mol,在催化剂条件下进行反应3小时.实验数据见下表:
序号 | 第一组 | 第二组 | 第三组 | 第四组 |
t/℃ | 30 | 40 | 50 | 80 |
NH3生成量/(10﹣6mol) | 4.8 | 5.9 | 6.0 | 2.0 |
第四组实验中以NH3表示反应的速率是_____,与前三组相比,NH3生成量最小的原因可能是______.
(4)氨水是实验室常用的弱碱.
①往CaCl2溶液中通入CO2至饱和,无明显现象.再通入一定量的NH3后产生白色沉淀,此时溶液中一定有的溶质是_____.请用电离平衡理论解释上述实验现象________________________.
②向盐酸中滴加氨水至过量,该过程中离子浓度大小关系可能正确的是______.
a.c(C1﹣)=c(NH4+)>c(H+)=c(OH﹣)
b.c(C1﹣)>c(NH4+)=c(OH﹣)>c(H+)
c.c(NH4+)>c(OH﹣)>c(C1﹣)>c(H+)
d.c(OH﹣)>c(NH4+)>c(H+)>c(C1﹣)