题目内容
下列离子方程式,正确的是( )
| A、等物质的量的SO2与氢氧化钠溶液反应:SO2+OH-=HSO3- | ||||
| B、用食醋除去水瓶中的水垢:CO32-+2CH3COOH=2CH3COO-+CO2+H2O | ||||
| C、已知电离平衡常数:H2CO3>HClO>HCO3-,向NaClO溶液中通入少量二氧化碳:2ClO-+CO2+H2O=2HClO+CO32- | ||||
D、用铜做电极电解CuSO4溶液:2Cu2++2H2O
|
考点:离子方程式的书写
专题:离子反应专题
分析:A.二氧化硫与氢氧化钠物质的量相等,反应生成亚硫酸氢钠;
B.水垢的主要成分为碳酸钙,碳酸钙在离子方程式中不能拆开,应该保留化学式;
C.次氯酸的酸性大于碳酸氢根离子,次氯酸钠与二氧化碳反应生成碳酸氢根离子;
D.铜为电解,阳极铜放电,电解质溶液中含有铜离子,阴极铜离子得到电子,该反应实质为单键精炼铜或电镀铜.
B.水垢的主要成分为碳酸钙,碳酸钙在离子方程式中不能拆开,应该保留化学式;
C.次氯酸的酸性大于碳酸氢根离子,次氯酸钠与二氧化碳反应生成碳酸氢根离子;
D.铜为电解,阳极铜放电,电解质溶液中含有铜离子,阴极铜离子得到电子,该反应实质为单键精炼铜或电镀铜.
解答:
解:A.等物质的量的SO2与氢氧化钠溶液反应生成亚硫酸氢钠,反应的离子方程式为:SO2+OH-=HSO3-,故A正确;
B.用食醋除去水瓶中的水垢,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.向NaClO溶液中通入少量二氧化碳,由于次氯酸酸性大于碳酸氢根离子,反应生成次氯酸和碳酸氢根离子,正确的离子方程式为:ClO-+CO2+H2O=HClO+HCO3-,故C错误;
D.用铜做电极电解CuSO4溶液,阳极铜失去电子生成铜离子,阴极硫酸铜溶液中的铜离子得到电子生成铜,阳极不是氢氧根离子放电,故D错误;
故选A.
B.用食醋除去水瓶中的水垢,碳酸钙不能拆开,正确的离子方程式为:CaCO3+2CH3COOH=Ca2++H2O+CO2↑+2CH3COO-,故B错误;
C.向NaClO溶液中通入少量二氧化碳,由于次氯酸酸性大于碳酸氢根离子,反应生成次氯酸和碳酸氢根离子,正确的离子方程式为:ClO-+CO2+H2O=HClO+HCO3-,故C错误;
D.用铜做电极电解CuSO4溶液,阳极铜失去电子生成铜离子,阴极硫酸铜溶液中的铜离子得到电子生成铜,阳极不是氢氧根离子放电,故D错误;
故选A.
点评:本题考查了离子方程式的正误判断,为中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法:检查反应能否发生,检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合守恒关系(如:质量守恒和电荷守恒等),选项D为易错点,注意电解池的阳极材料.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
某氮肥样品可能含有NH4HCO3、NH4Cl、NH4NO3中的一种或几种.称取该样品0.5000g,溶解配成100.00mL溶液,加过量浓NaOH溶液,加热,将产生的氨气通入60.00mL 0.1000mol?L-1的H2SO4溶液中(设产生的NH3全部逸出),剩余的H2SO4溶液能消耗20.00mL 0.2250mol?L-1的NaOH溶液.下列说法正确的是( )
| A、吸收NH3消耗的H2SO4为6.000×10-3mol |
| B、上述过程共产生NH3 268.8mL |
| C、该样品中NH4+的质量分数为43.2% |
| D、该氮肥样品必含NH4Cl |
已知3.01×1023个X气体分子的质量为8g,则X气体的摩尔质量是( )
| A、16g |
| B、32g |
| C、32g/mol |
| D、16g/mol |
一定条件下某容器中各微粒在反应前后的变化如图所示,其中●和○代表不同元素的原子.关于此反应说法错误的是( )


| A、一定属于可逆反应 |
| B、一定属于化合反应 |
| C、一定属于氧化还原反应 |
| D、一定属于放热反应 |
下列变化中,能一步实现的是( )
| A、SO2→H2SO3 |
| B、SiO2→H2SiO3 |
| C、NO2→HNO3 |
| D、S→SO3 |
电化学在日常生活中用途广泛,下图①是镁、次氯酸钠燃料电池的示意图,电池总反应式为:Mg+ClO-+H2O═Cl-+Mg(OH)2↓,图②是含Cr2O72-工业废水的电化学处理示意图.下列说法正确的是( )
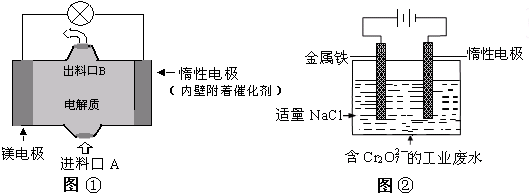

| A、图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去 |
| B、图②中阳极上的电极反应式为:Fe-3e-═Fe3+ |
| C、图①中发生的还原反应是:Mg2++ClO-+H2O+2e-═Cl-+Mg (OH)2↓ |
| D、若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀 |
下列类比关系正确的是( )
| A、AlCl3与过量NaOH溶液反应生成[Al(OH)4]-,则与过量NH3?H2O反应也生成[Al(OH)4]- |
| B、Al与Fe2O3能发生铝热反应,则与MnO2也能发生铝热反应 |
| C、Fe与Cl2反应生成FeCl3,则与I2反应可生成FeI3 |
| D、Na2O2与CO2反应生成Na2CO3和O2,则与SO2反应可生成Na2SO3和O2 |