题目内容
3.金属元素广泛存在与各种矿石和海水中,不同金属的冶炼方法各不相同.下列关于金属冶炼说法正确的是( )| A. | 不同金属的冶炼方法选择的原则主要是依据金属离子得电子的能力 | |
| B. | 金属的冶炼都是置换反应 | |
| C. | 应该大力开发金属矿物资源以满足人类生产生活的需要 | |
| D. | 工业上从海水中提取镁:海水$\stackrel{石灰乳}{→}$Mg(OH)2$\stackrel{灼烧}{→}$MgO$\stackrel{电解}{→}$Mg |
分析 A.金属的活动性不同,其金属阳离子得电子能力不同,根据金属活动性强弱判断金属冶炼方法;
B.金属的冶炼不一定是置换反应,也可能是分解反应;
C.金属矿物资源储量是有限的,要合理开发;
D.工业上采用电解熔融氯化镁方法冶炼镁.
解答 解:A.金属的活动性不同,其金属阳离子得电子能力不同,根据金属活动性强弱判断金属冶炼方法,如活泼金属采用电解方法、较活泼金属采用热氧化还原法等,所以不同金属的冶炼方法选择的原则主要是依据金属离子得电子的能力,故A正确;
B.金属的冶炼不一定是置换反应,也可能是分解反应,如MgCl2$\frac{\underline{\;电解\;}}{\;}$Mg+Cl2↑,故B错误;
C.金属矿物资源储量是有限的,要合理开发,不能造成资源浪费,故C错误;
D.MgO的熔沸点较高,如果采用电解熔融MgO冶炼Mg,会浪费大量能源,所以工业上采用电解熔融氯化镁方法冶炼镁,故D错误;
故选A.
点评 本题考查金属的冶炼,为高频考点,明确金属活泼性强弱与冶炼方法的关系是解本题关键,会根据金属活泼性强弱选取合理的冶炼方法,注意:不能采用电解氯化铝方法冶炼Al,因为熔融状态下氯化铝不导电.

练习册系列答案
相关题目
14.关于下列图示的说法中正确的是( )
| A. |  用如图所示实验可比较氯、碳、硅三种元素的非金属性强弱 | |
| B. | 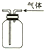 用如图所示实验装置通过排空气法收集C2H4气体 | |
| C. |  如图所示装置可用于制取乙酸乙酯,分液漏斗中装的是乙醇 | |
| D. | 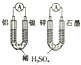 如图两个装置中提供导线的电子数相同时,生成H2的物质的量也相同 |
11.下列说法正确的是( )
| A. | 淀粉和纤维素在人体内均可水解生成葡萄糖 | |
| B. | 溴乙烷在浓硫酸、加热的条件下发生消去反应生成乙烯 | |
| C. | 乙烯、苯分子中都含有碳碳双键,都能发生加成反应 | |
| D. | 饱和Na2SO4溶液和浓硝酸均可使蛋白质溶液产生沉淀,但原理不同 |
18.下列关于碳氢化合物的叙述正确的是( )
| A. | 碳氢化合物的通式为CnH2n+2 | |
| B. | 烷烃中都有碳碳单键 | |
| C. | 烷烃分子中的碳原子只能在一条链上,不能出现支链 | |
| D. | 烷烃分子中可能出现n个甲基(n=1,2,3…) |
8.A、B、C、D为四种短周期元素,已知A、C同主族,B、C、D同周期,:A的气态氢化物比C的气态氢化物稳定;B的阳离子比D的阳离子氧化性强;B的阳离子比C的阴离子少一个电子层.下列叙述中正确的是( )
| A. | 原子序数:B>D>A>C | B. | 单质熔点:D>B,A>C | ||
| C. | 原子半径:D>B>C>A | D. | 简单离子半径:D>B>C>A |
15.下列叙述不正确的是( )
| A. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次降低 | |
| B. | 制备纯净的氯乙烷可用等物质的量乙烷和氯气在光照条件下反应 | |
| C. | 等物质的量的乙烷、乙烯和苯分别在氧气中充分燃烧,消耗氧气最多的是苯 | |
| D. | 用18O标记的CH3CH218OH与乙酸反应制取乙酸乙酯,当反应达到平衡时,18O存在于水、乙醇以及乙酸乙酯 |
12.阿伏加德罗常数的值为NA,下列叙述中错误的是( )
①3.2g O2和O3的混合气中含有的氧原子数目为0.2NA
②含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
③7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA
④标准状况下,22.4LC6H6(苯)的分子数目为NA
⑤1L 0.1mol/L的 Al2(SO4)3溶液中,Al3+的数目为0.2NA.
①3.2g O2和O3的混合气中含有的氧原子数目为0.2NA
②含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA
③7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1NA
④标准状况下,22.4LC6H6(苯)的分子数目为NA
⑤1L 0.1mol/L的 Al2(SO4)3溶液中,Al3+的数目为0.2NA.
| A. | ①②③④⑤ | B. | ①③④⑤ | C. | ②③④⑤ | D. | ③④⑤ |
13.下列反应的化学方程式错误的是( )
| A. | 苯与液溴制溴苯的反应: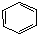 +Br2$\stackrel{FeBr_{3}}{→}$ +Br2$\stackrel{FeBr_{3}}{→}$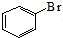 +HBr +HBr | |
| B. | 乙酸与乙醇的酯化反应:CH3COOH+CH3CH2${\;}_{\;}^{18}$OH$→_{△}^{浓H_{2}SO_{4}}$CH3CO${\;}_{\;}^{18}$OCH2CH3+H2O | |
| C. | 溴乙烷与NaOH水溶液混和共热 CH3CH2Br+NaOH$→_{△}^{水}$CH2=CH2+H2O+NaBr | |
| D. | 乙醇的消去反应 CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O |