题目内容
【题目】[2019·武汉市武昌区高三五月调研考试]室温下,用0.100 mol·L1的NaOH溶液分别滴定均为20.00mL0.100 mol·L1的HCl溶液和醋酸溶液,滴定曲线如图所示。下列说法正确的是
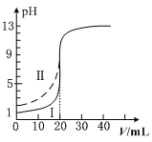
A. Ⅰ表示的是滴定醋酸的曲线
B. pH=7时,滴定醋酸消耗的V(NaOH)>20.00mL
C. V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-)
D. V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
【答案】C
【解析】
A. 未滴加NaOH溶液时,0.1mol/L盐酸pH=1,0.1mol/L醋酸pH>1,所以滴定盐酸的曲线是图Ⅰ,故A错误;
B. V(NaOH)=20.00mL时恰好生成醋酸钠,溶液呈碱性,若pH=7,则加入的氢氧化钠溶液体积应该稍小,即V(NaOH)<20.00mL,故B错误;
C. V(NaOH)=20.00mL时,二者反应生成氯化钠和醋酸钠,醋酸根发生水解,浓度小于氯离子,即c(Cl-)>c(CH3COO-),故C正确;
D. V(NaOH)=10.00mL时,与醋酸反应后得到等浓度的醋酸和醋酸钠的混合溶液,由于醋酸的电离程度大于醋酸根离子的水解程度,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒可知:c(CH3COO-)>c(Na+),溶液中正确的离子浓度大小为:c(CH3COO-)>c(Na+)>c(H+)>c(OH-),故D错误;
故选C。

练习册系列答案
相关题目